Authors: Σχιζοδήμος Θ.1 MD, Σουλούντση Β.2 MD
1 Β΄ Μ.Ε.Θ Γ.Π.Ν «Γ.ΠΑΠΑΝΙΚΟΛΑΟΥ»,ΘΕΣΣΑΛΟΝΙΚΗ
2 Α΄ Μ.Ε.Θ Γ.Π.Ν «Γ.ΠΑΠΑΝΙΚΟΛΑΟΥ»,ΘΕΣΣΑΛΟΝΙΚΗ
Abstract
Bloodstream infections (BSIs) are a frequent and life threatening condition in hospital settings. The case fatality rate associated with BSI reaches 35-50% when associated with admission to intensive care unit (ICU). The extensive use of intravascular catheters, however, is recognized as the most important factor contributing to the occurrence of BSI. Catheter-related BSIs (CR-BSIs) are the most common types of BSI in ICU. Bacteraemias that occur in the ICU are classified as Community Onset BSI and Hospital Acquired (HA) BSI. They are also distinguished in primary and secondary. Community-onset BSIs are those that occur in outpatients or are first identified 48 h after admission to hospital/ICU, and they may be sub classified further as health care associated (HCA), when they occur in patients with significant prior health care exposure, or community associated, in other cases. Hospital Acquired (HA) and / or ICU-acquired BSIs are defined as those occurring more than 48 hours after the patient’s admission into the hospital or ICU or within 48 hours of leaving the hospital or the ICU. Community acquired BSIs usually due to susceptible bacteria should be clearly differentiated from HCA and HA BSIs frequently due to resistant hospital strains. A bedridden status, presence of indwelling devices, recent hospitalization or contact with health care facilities and recent antibiotic therapy may represent the most important risk factors for the development of emerging multi drug resistant (MDR) GN infections. The basic components of the treatment of a bacteraemia in the ICU are determining the type of bacteraemia in order to target potential pathogens, the initiation of empirical antimicrobial therapy based on the guidelines, and the source control if it is a secondary bacteremia. These goals become difficult to achieve in case of BSI due to multi-drug resistant pathogens with high MICs to antimicrobials. The main mechanisms which have put in danger the marvelous antibiotic weapon are the production of ESBL (several different subtypes), the production of carbapenemases and metallo-betalactamases, with consequent spread of multi or pan-resistant organism and the emerging growing resistance in colistin. The targeted treatment should be applied immediately after receiving the susceptibility test from the cultures. Targeted treatment essentially consists in redefining antibiotic treatment, in de-escalation in order to decrease the antibiotic selection pressure, and in determining the duration of treatment. Source control is recognized as an important part of the therapy of BSIs and has been recently shown to be independently related with outcome. Depending on the source of the infection (pneumonia, CRBSIs, urinary tract infections, intra-abdominal infections), the therapeutic strategy should be based on international guidelines in combination with local microbiology and local antibiotic resistance data.
ΕΙΣΑΓΩΓΗ
Οι λοιμώξεις αιματικής ροής (Blood Stream Infections, BSI) αποτελούν σημαντικό αίτιο νοσηρότητας και θνητότητας παγκοσμίως, και ιδιαίτερα στη μονάδα εντατικής θεραπείας (ΜΕΘ) τα ποσοστά θνητότητας μπορεί να φτάσουν το 30-50%1,2. Η εκτεταμένη χρήση των κεντρικών φλεβικών καθετήρων (ΚΦΚ) και αρτηριακών γραμμών στη ΜΕΘ αναγνωρίζεται ως ένας επιπλέον επιβαρυντικός παράγοντας που συντελεί στην αύξηση της επίπτωσης των BSI2-6. H μεγάλη αύξηση των πολυανθεκτικών μικροβίων και η αναδυόμενη, ολοένα αυξανόμενη, αντίσταση στα αντιβιοτικά διογκώνει περαιτέρω το πρόβλημα, καθώς η αντιβιοτική θεραπεία αποτελεί τον ακρογωνιαίο λίθο της αντιμετώπισης αυτών των λοιμώξεων. Έτσι, η εμπειρική θεραπεία πολλές φορές κρίνεται αναποτελεσματική, συντελώντας στην αύξηση της νοσηρότητας και θνητότητας των BSI7,8.
Ως λοιμώξεις αιματικής ροής ορίζονται οι λοιμώξεις που καθορίζονται από την παρουσία ενός βιώσιμου μικροβιακού μικροοργανισμού ή μύκητα στο αίμα (η οποία τεκμηριώνεται με την παρουσία μιας ή περισσότερων θετικών αιμοκαλλιεργειών), με σύγχρονη εκδήλωση φλεγμονώδους αντίδρασης στον οργανισμό, η οποία χαρακτηρίζεται από μεταβολή των κλινικών, εργαστηριακών και αιμοδυναμικών παραμέτρων9. Η παρουσία κλινικο-εργαστηριακών δεδομένων λοίμωξης είναι απαραίτητη προκειμένου να διαφοροδιαγνωστούν οι BSI τόσο από την παροδική βακτηριαιμία ή μυκηταιμία (οι οποίες δεν σχετίζονται με λοίμωξη) όσο και από την επιμόλυνση. Στην τελευταία, παρατηρείται ανάπτυξη θετικών καλλιεργειών για μικροοργανισμούς που δεν είναι παρόντες στο αίμα, αλλά είναι αποτέλεσμα ανεπαρκούς ασηψίας/αντισηψίας κατά την λήψη ή την διαδικασία καλλιέργειας των ληφθέντων δειγμάτων στο εργαστήριο.
Ανάλογα με την ανοσιακή κατάσταση του ξενιστή οι BSI μπορούν να εκδηλωθούν σε τέσσερις κύριες ομάδες ασθενών:
- σε ανοσολογικά φυσιολογικούς ξενιστές που διατηρούν ακέραια την άμυνα τους
- σε ασθενείς με ανώριμο ή «γερασμένο» ανοσοποιητικό σύστημα (νεογέννητα, ηλικιωμένοι)
- σε ασθενείς που πάσχουν από παθολογικές καταστάσεις ή λαμβάνουν φαρμακολογικές θεραπείες που προδιαθέτουν σε λοιμώξεις
- σε ασθενείς που ανήκουν στην ευρύτερη κατηγορία των σχετιζόμενων με την φροντίδα υγείας ή το νοσοκομείο λοιμώξεων.
Βασικοί άξονες στη διαχείριση αυτών των λοιμώξεων αποτελούν η γρήγορη διαγνωστική προσέγγιση και η ορθή αντιμετώπιση τους.
Βακτηριαιμίες-Ταξινόμηση
Οι βακτηριαιμίες αποτελούν ειδική κατηγορία των BSI και οφείλονται στην παρουσία μικροβιακού παράγοντα στο αίμα. Οι βακτηριαιμίες που εκδηλώνονται στη ΜΕΘ (Σχήμα 1) ταξινομούνται σε αυτές που «προέρχονται» από την κοινότητα (Community Onset BSI) και σε αυτές που «αποκτώνται» στο νοσοκομείο (Hospital Acquired, HA). Στις τελευταίες εντάσσονται και αυτές που «αποκτώνται» στην ΜΕΘ (ICU acquired BSI)10,11. Στις Community Onset BSI, εκτός από αυτές που «αποκτώνται» στην κοινότητα (Community Acquired BSI, CA-BSI), τελευταία, αναγνωρίζεται και μια νέα υποκατηγορία, οι βακτηριαιμίες που εκδηλώνονται σε αρρώστους κοινότητας αλλά σχετίζονται με το σύστημα φροντίδας υγείας (Health Care Acquired Community Onset BSI, HCA-BSI). Οι τελευταίες αναφέρονται σε κάθε ασθενή που κατά τις προηγούμενες 30 μέρες πριν την εμφάνιση της BSI νοσηλεύτηκε σε νοσηλευτικό ίδρυμα ή σε ίδρυμα μακράς διάρκειας φροντίδας, σε ασθενή που έλαβε ενδοφλέβια θεραπεία ή χημειοθεραπεία, παρεντερική διατροφή, ειδική νοσηλευτική κατ’ οίκον φροντίδα, ή υπεβλήθη σε αιμοδιάλυση ή περιποίηση τραύματος. Επίσης, αφορούν οποιονδήποτε ασθενή είχε νοσηλεία σε νοσοκομείο για 48 ή περισσότερες ώρες κατά τις προηγούμενες 90 μέρες πριν την εμφάνιση της BSI 11,12. Ουσιαστικά οι λοιμώξεις αυτές εκδηλώνονται σε ασθενείς κοινότητας με σημαντικές συνοσηρότητες, και παρουσιάζουν κλινικά, μικροβιολογικά δεδομένα και στοιχεία έκβασης παρόμοια με αυτά των νοσοκομειακών BSI13.
| ΒΑΚΤΗΡΙΑΙΜΙΕΣ ΣΤΗ ΜΕΘ | |
| ΚΟΙΝΟΤΗΤΑΣ
(Community Onset) |
Community Acquired |
| Health Care Acquired | |
| ΕΝΔΟ-ΝΟΣΟΚΟΜΕΙΑΚΕΣ | Νοσοκομειακές
(Hospital Acquired) |
| ΜΕΘ
(ICU acquired) |
|
Ορισμοί
Ως σχετιζόμενες με την κοινότητα (Community Onset) βακτηριαιμίες ορίζονται αυτές που εμφανίζονται πριν ή/ και εντός των πρώτων 48 ωρών από την είσοδο του ασθενούς στο νοσοκομείο ή στη ΜΕΘ. Διακρίνονται σε πρωτοπαθείς και δευτεροπαθείς. Στις πρώτες η θετική αιμοκαλλιέργεια δεν σχετίζεται με αποδεδειγμένη απομακρυσμένη λοίμωξη, και απαντώνται σε ποσοστό περίπου 40%. Στις δευτεροπαθείς υπάρχει, αποδεδειγμένα, λοίμωξη με τον ίδιο μικροοργανισμό σε άλλο σημείο του σώματος, με συνηθέστερες εντοπίσεις το κατώτερο αναπνευστικό, το ουροποιογεννητικό ή κάποια ενδοκοιλιακή λοίμωξη (δευτεροπαθής περιτονίτιδα, ενδοκοιλιακά αποστήματα, χολαγγειίτιδα, παγκρεατίτιδα).
Ως νοσοκομειακές (Hospital Acquired, HA) ή/και σχετιζόμενες με την ΜΕΘ (ICU acquired) βακτηριαιμίες ορίζονται αυτές που εμφανίζονται πάνω από 48 ώρες από την εισαγωγή του ασθενούς στο νοσοκομείο ή στη ΜΕΘ ή μέσα σε 48 ώρες από την αποχώρηση του από το νοσοκομείο ή την ΜΕΘ. Διακρίνονται, επίσης, σε πρωτοπαθείς και δευτεροπαθείς. Σύμφωνα με την μελέτη Eurobact14 ως συνηθέστερες αιτίες δευτεροπαθούς βακτηριαιμίας στο νοσοκομείο/ΜΕΘ αναγνωρίζονται οι λοιμώξεις αιματικής ροής που σχετίζονται με τον ΚΦΚ (Catheter Related BSI, CRBSI) (σε ποσοστό 21.4%), οι λοιμώξεις του αναπνευστικού (σε ποσοστό 21.1%), ενώ σε ένα σημαντικό ποσοστό (23.9%) δεν αναγνωρίζεται η εστία της λοίμωξης.
Για την διάγνωση των CRBSI είναι απαραίτητη η παρουσία κλινικών σημείων λοίμωξης και η απομόνωση του ιδίου μικροοργανισμού από:
- Τουλάχιστον μία καλλιέργεια περιφερικού αίματος και το άκρο του ΚΦΚ (ημιποσοτική > 15 cfu ή ποσοτική > 102 cfu/ml) (ΑI) ή
- Ποσοτικές καλλιέργειες αίματος σε μια αναλογία > 3:1 cfu/ml του αίματος που λαμβάνεται μέσα από τον ΚΦΚ σε σχέση με αυτό που λαμβάνεται από περιφερικό σημείο (ΑΙΙ) ή
- Ανάπτυξη μικροοργανισμού σε αιμοκαλλιέργεια που ελήφθη μέσω ΚΦΚ τουλάχιστον 2 ώρες νωρίτερα από καλλιέργεια (ιδίου όγκου αίματος) που ελήφθη από περιφερικό αίμα (ΑΙΙ) (Differential Time To Positivity, DTTP)15
Οι CRBSI μπορεί να αναφέρονται στους μικρής διάρκειας (Short Term Catheters) ή στους μακράς διάρκειας ΚΦΚ (Long Term Catheters). Οι πρώτοι αποτελούν ΚΦΚ που προορίζονται για προσωρινή χρήση και δεν έχουν υποδόριο τμήμα-σήραγγα (tunnel), ούτε είναι πλήρως εμφυτεύσιμοι ενώ οι δεύτεροι προορίζονται να παραμείνουν στη θέση τους για παρατεταμένο ή αόριστο χρονικό διάστημα, έχουν υποδόριο tunnel ή είναι πλήρως εμφυτεύσιμοι.
Για λόγους επιτήρησης, στις CRBSI ταξινομούνται επίσης και οι λοιμώξεις στο σημείο εξόδου του ΚΦΚ. Για την διάγνωση της τελευταίας είναι απαραίτητη η παρουσία κλινικών σημείων λοίμωξης (ερύθημα, τάση, σκληρία δέρματος, διαπύηση) με ακτίνα μέχρι 2 cm από το σημείο εξόδου, με ή χωρίς παρουσία σημείων ή συμπτωμάτων λοίμωξης (πυρετός ή πυώδη παροχέτευση από το σημείο εξόδου), με ή χωρίς συνοδό μικροβιαιμία15.
Ως λοίμωξη υποδόριου τμήματος (tunnel infection) ορίζεται η παρουσία ευαισθησίας, ερυθήματος, και/ή σκληρία δέρματος με ακτίνα > 2 cm από το σημείο εξόδου του καθετήρα με υποδόριο τμήμα (π.χ Hickman ή Broviac) με ή χωρίς μικροβιαιμία15.
Η λοίμωξη της θήκης (Pocket Infection) εκδηλώνεται με παρουσία επιμολυνθέντος υγρού στην υποδόρια θήκη μιας ολικώς εμφυτευθείσας ενδαγγειακής συσκευής. Συχνά συνοδεύεται από ευαισθησία, ερύθημα και/ή σκληρία ύπερθεν της θήκης ή από αυτόματη ρήξη και παροχέτευση ή νέκρωση του υπερκείμενου δέρματος, με ή χωρίς μικροβιαιμία15.
Παράγοντες κινδύνου- Χρόνος εκδήλωσης
Ως παράγοντες κινδύνου για την εκδήλωση βακτηριαιμιών στο νοσοκομείο/ΜΕΘ έχουν αναγνωριστεί το υψηλό APACHE II score στην εισαγωγή, η παρουσία μηχανικού αερισμού, η θεραπεία υποκατάστασης νεφρικής λειτουργίας, το πρόσφατο χειρουργείο, η ανοσοκαταστολή και οι ενδαγγειακοί καθετήρες (ΚΦΚ, αρτηριακοί καθετήρες)16.
Για την ανάπτυξη των CRBSI αναγνωρίζονται παράγοντες κινδύνου που σχετίζονται με τον ασθενή, με τον καθετήρα ή την διαχείρισή του. Στους πρώτους συγκαταλέγονται η σοβαρότητα της νόσου, η διαταραγμένη ακεραιότητα του δέρματος, η ουδετεροπενία και η παρουσία απομακρυσμένης λοίμωξης. Σε ότι αφορά τον ΚΦΚ, μεγάλη σημασία φαίνεται να έχει η ανατομική θέση αυτού και ο αριθμός των αυλών. Οι υποκλείδιοι ή σφαγιτιδικοί καθετήρες θεωρείται ότι συνδέονται με χαμηλότερο αριθμό λοιμώξεων έναντι των μηριαίων, αν και πρόσφατη μετα-ανάλυση δεν έδειξε κάποιο όφελος για τους πρώτους έναντι των τελευταίων17. Η παρουσία πολλαπλών αυλών συνδέεται με μεγαλύτερο κίνδυνο λοιμώξεων έναντι των ΚΦΚ με μονό αυλό. Θεμελιώδης, βέβαια, για την αποφυγή των CRBSI φαίνεται να είναι η συμμόρφωση με τις κατευθυντήριες οδηγίες18 σε ότι αφορά τις ενδείξεις αντικατάστασης, την άσηπτη τεχνική τοποθέτησης και συντήρησης ενός ΚΦΚ.
Ο μέσος χρόνος εκδήλωσης των ενδονοδοκομειακών βακτηριαιμιών είναι 14 ημέρες (7-26 ημέρες). Το 76% αυτών εκδηλώνονται στη ΜΕΘ με μέσο χρόνο εμφάνισης τις 8 ημέρες ( 3-16 ημέρες)14. Η θνητότητα τους είναι περίπου 15-20%, και μπορεί να φτάσει το 35-50% όταν το επεισόδιο της βακτηριαιμίας σχετίζεται με εισαγωγή στη ΜΕΘ1.
Επιδημιολογικά και μικροβιολογικά δεδομένα των βακτηριαιμιών
Το μέγεθος του προβλήματος είναι μεγάλο. Σύμφωνα με την μελέτη EPICII19 οι βακτηριαιμίες αποτελούν την 3η αιτία των ενδονοσοκομειακών λοιμώξεων, μετά τις λοιμώξεις αναπνευστικού και τις ενδοκοιλιακές. Σε πρόσφατη μελέτη των Ammerlaan et al, που αφορούσε καταγραφή 33000 βακτηριαιμιών στη διάρκεια μιας δεκαετίας, σημειώθηκε μεγάλη αύξηση της μέσης επίπτωσής τους (από 3.8 ως 24.4/ 100 000 ασθενείς-ημέρες)20.
Οι CRBSI διογκώνουν ακόμη περισσότερο το πρόβλημα, αν συνυπολογίσουμε, με βάση συστηματική ανασκόπηση της βιβλιογραφίας, ότι περισσότερες από 250000 CRBSI εμφανίζονται κάθε χρόνο στις ΗΠΑ και πάνω από το ένα τρίτο αυτών αφορούν την ΜΕΘ21,22. Θεωρείται ότι αποτελούν το πιο σημαντικό αίτιο των ενδονοσοκομειακών μικροβιαιμιών. Πιο πρόσφατα δεδομένα θεωρούν ότι αποτελούν το 30% περίπου των βακτηριαιμιών στο νοσοκομείο23,24. Αποτελούν λοιμώξεις που αυξάνουν και την διάρκεια νοσηλείας και το κόστος νοσηλείας21 και, ενδεχομένως, αυξάνουν και τον κίνδυνο θανάτου25, 26. Η θνητότητα τους κυμαίνεται από 192 έως 34% 24.
α. Επιδημιολογικά και μικροβιολογικά δεδομένα των σχετιζόμενων με την κοινότητα βακτηριαιμιών
Οι σχετιζόμενες με την κοινότητα βακτηριαιμίες αποτελούν σημαντικό τμήμα των ενδονοσοκομειακών βακτηριαιμιών. Πρόσφατες μελέτες13,27, που κατέγραψαν και μελέτησαν το πρώτο επεισόδιο βακτηριαιμίας μετά την εισαγωγή στο νοσοκομείο ή τη ΜΕΘ, έδειξαν ότι πάνω από το 60% των μικροβιαιμιών κατατάσσονταν στις σχετιζόμενες με την κοινότητα βακτηριαιμίες (Εικόνα 1), ενώ τα πιο συχνά παθογόνα ήταν Escherichia coli, Staphylococcus aureus και Streptococcus pneumoniae. Πάντως, σε ότι αφορά τις HCA βακτηριαιμίες φαίνεται ότι η μικροβιολογία τους, όπως και η πιθανότητα απομόνωσης ανθεκτικού στα αντιβιοτικά παθογόνου, είναι παρόμοια με αυτή των νοσοκομειακών13. Πράγματι, οι Laupland et al28, σε πρόσφατη ανασκόπηση της βιβλιογραφίας, έδειξαν ότι οι HCA-BSI συγκρινόμενες με τις CA-BSI έχουν υψηλότερα ποσοστά Staphylococcus aureus και Pseudomonas aeruginosa και χαμηλότερα ποσοστά Streptococcus pneumoniae και Escherichia coli. Επίσης, είναι συχνότερες σε πιο ηλικιωμένους με συνοσηρότητες, έχουν μεγαλύτερη διάρκεια παραμονής στο νοσοκομείο, έχουν υψηλότερα ποσοστά αντιμικροβιακής αντίστασης, και έχουν πιο αυξημένη θνητότητα.

Εικόνα 1. Ταξινόμηση των BSA [δεδομένα από βιβλιογραφικές αναφορές 13: Vallés J et al (2011) και 27: Lenz R et al (2012)].
β. Επιδημιολογικά και μικροβιολογικά δεδομένα των νοσοκομειακών βακτηριαιμιών
Η επιδημιολογία-μικροβιολογία τωνHA βακτηριαιμιών είναι διαφορετική από αυτή των σχετιζόμενων με την κοινότητα και έχει μεταβληθεί στη διάρκεια των τελευταίων δεκαετιών. Οι Wisplinghoff et.al29 σε καταγραφή 24176 επεισοδίων BSI, έδειξαν ότι περισσότερο από 60% των παθογόνων ήταν Gram θετικά (κοαγκουλάση αρνητικοί σταφυλόκοκκοι, χρυσίζων σταφυλόκοκκος και εντερόκοκκοι), ενώ η ανάπτυξη ανθεκτικών Gram αρνητικών βακτηριδίων εκδηλωνόταν, συνήθως, μετά την 21η μέρα της νοσηλείας. Στην EPICII μελέτη19 τα μικροβιολογικά δεδομένα διαφοροποιούνται σημαντικά. Τα Gram αρνητικά βακτηρίδια αποτελούσαν το 62% των παθογόνων της σήψης, έναντι 47% των Gram θετικών. Παρόμοια δεδομένα προκύπτουν και σε πιο πρόσφατες μελέτες13,14,30, ενώ μεμονωμένες μόνο εργασίες2,23 αναδεικνύουν υπεροχή των gram θετικών, γεγονός που μπορεί να σχετίζεται με την τοπική επιδημιολογία των ΜΕΘ (Εικόνα 2). Παρόμοια είναι τα στοιχεία που προέρχονται από 29 ελληνικές ΜΕΘ31. Σε καταγραφή των πρώτων 288επεισοδίων BSI που αποκτήθηκαν στη ΜΕΘ ή μέσα σε 48 ώρες πριν την εισαγωγή στη ΜΕΘ,η υπεροχή των Gram αρνητικών βακτηριδίων είναι ξεκάθαρη (Εικόνα 3).
Η επίπτωση των CRBSI, εκφραζόμενη ως αριθμός λοιμώξεων ανά 1000 μέρες καθετηριασμού, ποικίλλει από 0.1 έως 2.7 ανά 1000 μέρες καθετηριασμού 21,32. Η μεγαλύτερη επίπτωση παρατηρείται στους μικρής διάρκειας ΚΦΚ(2.7 ανά 1000 μέρες καθετηριασμού)21. Τα μικρόβια που ευθύνονται για τις CRBSI κατά φθίνουσα σειρά είναι: σταφυλόκοκκοι (Staphylococcus aureus, coagulase-αρνητικοί σταφυλόκοκκοι), εντερόκοκκοι, αερόβια gram αρνητικά βακτήρια, μύκητες. Πάντως, όταν τα αερόβια gram αρνητικά βακτήρια θεωρηθούν ως ομάδα, αποτελούν την δεύτερη αιτία των CRBSI μετά τους σταφυλόκοκκους . Στην αιτιολογία των CRBSI σημαντικό ρόλο παίζουν τα χαρακτηριστικά του ξενιστή, η θεραπεία που ακολουθεί ο ασθενής, η θέση του καθετήρα και η τοπική επιδημιολογία. Στους ασθενείς που υποβάλλονται σε αιμοκάθαρση επικρατεί ο staphylococcus aureus ενώ στους καρκινοπαθείς τα gram αρνητικά μικρόβια. Οι επιμολύνσεις των διαλυμάτων προάγουν τις λοιμώξεις από τα gram αρνητικά βακτήρια, ενώ η παρεντερική διατροφή ευνοεί τους μύκητες. Ο ΚΦΚ στην μηριαία φλέβα προδιαθέτει σε λοιμώξεις από gram αρνητικά βακτήρια και μύκητες. Είναι πάντως βασικό να τονιστεί ότι μεγάλη σημασία για την μείωση της επίπτωσης των CRBSI έχει η τήρηση σχολαστικών μέτρων προφύλαξης και η συμμόρφωση με τις κατευθυντήριες γραμμές πρόληψης αυτών33.

Εικόνα 1. Ταξινόμηση των BSA [δεδομένα από βιβλιογραφικές αναφορές 13: Vallés J et al (2011) και 27: Lenz R et al (2012)].

Εικόνα 3. Κατανομή παθογόνων BSI στις ελληνικές ΜΕΘ [δεδομένα από βιβλιογραφική αναφορά 31: Dimopoulos G et al (2015)].
γ. Επιδημιολογικά δεδομένα αντίστασης στα αντιβιοτικά
Η πιο μεγάλη αλλαγή στην επιδημιολογία των νοσοκομειακών βακτηριαιμιών τα τελευταία χρόνια είναι η ανάδυση των πολύ ανθεκτικών μικροοργανισμών, ειδικά των gram-, όπως P. aeruginosa, A. baumannii και Klebsiella pneumoniae34-37.Οι Ammerlaan et al 20 κατέγραψαν, στη διάρκεια μιας δεκαετίας, μια στατιστικά σημαντική αύξηση των βακτηριαιμιών, κυρίως, στα νοσοκομεία όπου ενδημούν οι λοιμώξεις από ανθεκτικά βακτήρια (από 4.6 μικροοργανισμοί ανά 100000 ημέρες ασθενών σε 29,1 μικροοργανισμοί ανά 100000 ημέρες ασθενών, p<0.001) με αύξηση της μέσης επίπτωσης των βακτηριαιμιών που οφείλονταν σε ανθεκτικά στα αντιβιοτικά βακτηρίδια κατά 20.6/ 100 000 ασθενείς-ημέρες, ανεξάρτητα από τις βακτηριαιμίες που προκαλούνταν από τα ευαίσθητα μικρόβια. Αυτό αποδόθηκε σε διαφορές είτε στην πολιτική πρόληψης των λοιμώξεων είτε στην συνταγογράφηση των αντιβιοτικών. Εξίσου ανησυχητικά είναι και τα δεδομένα από την μελέτη Eurobact14 τόσο για την απομόνωση πολυανθεκτικών (Multiple Drug Resistant, MDR)και Extended Spectrum Resistant (XDR) παθογόνων (50,7 vs 22%, αντίστοιχα) όσο και για τα υψηλά ποσοστά αντίστασης στις καρβαπενέμες (Eικόνες 4,5).

Εικόνα 4. Eurobact study [δεδομένα από βιβλιογραφική αναφορά 14: Tabah A et al (2012)].

Εικόνα 5. Eurobact study-Αντίσταση στις καρβαπανέμες [δεδομένα από βιβλιογραφική αναφορά 14: Tabah A et al (2012)].

Εικόνα 6. Παθογόνα BSI στις ελληνικές ΜΕΘ [δεδομένα από βιβλιογραφική αναφορά 31: Dimopoulos G et al (2015)].
Αντιμετώπιση βακτηριαιμιών
Τα βασικά συστατικά της θεραπευτικής αντιμετώπισης μιας βακτηριαιμίας στη ΜΕΘ, αμέσως μετά την λήψη τουλάχιστον δύο set καλλιεργειών αίματος, είναι:
- ο καθορισμός του τύπου της βακτηριαιμίας (αν είναι σχετιζόμενη με την κοινότητα ή ενδονοσοκομειακή και αν είναι πρωτοπαθής ή δευτεροπαθής), με βάση τους ισχύοντες ορισμούς,προκειμένου να προσανατολιστούμε στα πιθανά παθογόνα
- η έναρξη της αντιμικροβιακής θεραπείας με βάση τις κατευθυντήριες οδηγίες και
- ο έλεγχος της εστίας λοίμωξης, εφόσον, πρόκειται για δευτεροπαθή βακτηριαιμία.
Ι. ΑΝΤΙΜΙΚΡΟΒΙΑΚΗ ΘΕΡΑΠΕΙΑ
Είναι αδιαμφισβήτητο ότι κατά την έναρξη της αντιμικροβιακής θεραπείας, η χορήγηση κατάλληλης, επαρκούς και έγκαιρης εμπειρικής αντιβιοτικής θεραπείας είναι θεμελιώδους σημασίας. Οι Kumar et al 39 έδειξαν ότι ακατάλληλη αντιβιοτική θεραπεία χορηγήθηκε στο 20% των ασθενών με σηπτικό shock, και αυτή σχετίστηκε με 5πλάσια αύξηση της θνητότητας. Στην πρωτοπαθή μάλιστα αιματογενή λοίμωξη, που συνοδευόταν από σηπτικό shock, η ακατάλληλη αντιβιοτική θεραπεία μείωσε την επιβίωση κατά 17.6 φορές συγκριτικά με αυτούς που έλαβαν κατάλληλη. Ομοίως, οι Retamar et al 40 μελέτησαν 801 επεισόδια BSI και συμπέραναν ότι η ανεπαρκής αντιβιοτική θεραπεία συνδεόταν ανεξάρτητα με την αύξηση της θνητότητας στις 14 και 30 μέρες (p<0.001, p<0.02, αντίστοιχα). Οι Tabah et al14 κατέληξαν ότι η ανεπαρκής αντιβιοτική θεραπεία σχετιζόταν με την 28 ημερών θνητότητα ανεξάρτητα από την ηλικία, την χρόνια συνοσηρότητα, την σοβαρότητα της οξείας νόσου, την παρουσία shock και την δυσλειτουργία οργάνων. Η έγκαιρη αντιβιοτική θεραπεία είναι επίσης κεφαλαιώδους σημασίας. Οι Ferrer et al41 σε 18000 ασθενείς με σοβαρή σήψη και σηπτικό shock διαπίστωσαν ότι η θνητότητα αυξανόταν κατά 1% / ώρα όταν η θεραπεία ήταν επαρκής μετά την 6η ώρα (δηλ από 24.6% όταν η θεραπεία ήταν επαρκής μετά την 1η ώρα, στο 33.1% όταν η θεραπεία ήταν επαρκής μετά την 6η ώρα, p<0.001). Πάντως, στην αύξηση του χρόνου για επαρκή αντιμικροβιακή αγωγή και στην 28 ημερών θνητότητα συντελεί και η παρουσία ενός MDR, XDR ή PDR μικροοργανισμού14,42,43.
Για την επιλογήτης κατάλληλης εμπειρικής αντιβιοτικής θεραπείας θα πρέπει να λαμβάνονται σοβαρά υπόψη:
- τα χαρακτηριστικά του ασθενούς
- η βαρύτητα της λοίμωξης
- η εθνική και τοπική επιδημιολογία και η αντίσταση στα αντιβιοτικά, όπως αυτή καθορίζεται από τα ποσοστά απομόνωσης MDR, XDR, και PDR μικροοργανισμών, ειδικά για τις ενδονοσοκομειακές και τις HCA βακτηριαιμίες
- οι παράγοντες κινδύνου του ασθενούς για λοιμώξεις από ειδικά παθογόνα
Στην βιβλιογραφία έχουν περιγραφεί διάφορες μέθοδοι και συστήματα βαθμολόγησης προκειμένου να καθοριστούν οι ασθενείς που βρίσκονται σε κίνδυνο να αναπτύξουν λοιμώξεις από MDR παθογόνα34. Ωστόσο, η αξία των συστημάτων βαθμολόγησης είναι περιορισμένη44. Στην κλινική πράξη πρέπει να συνεκτιμώνται οι προηγούμενες καλλιέργειες και τα test ευαισθησίας των απομονωθέντων μικροοργανισμών και παράγοντες κινδύνου, οι οποίοι καθορίζουν την ανάγκη χρήσης ευρέως φάσματος αντιβιοτικής αγωγής. Παραδοσιακοί παράγοντες κινδύνου για λοίμωξη από MDR παθογόνα είναι οι τοπικές επιδημίες από MDR, ο προηγούμενος αποικισμός με MDR παθογόνα, η έκθεση σε ευρέως φάσματος αντιβιοτικά (κυρίως φθοριοκινολόνες και/ή 3ης γενιάς κεφαλοσπορίνες, και/ή καρβαπενέμες) τις τελευταίες 30 μέρες, η εισαγωγή στην ΜΕΘ, η παρουσία ΚΦΚ ή άλλης ενδαγγειακής συσκευής ή ουροκαθετήρα, το πρόσφατο χειρουργείο ή άλλες επεμβατικές διαδικασίες μέσα στις προηγούμενες 30 μέρες, η σοβαρότητα της υποκείμενης νόσου (Charlson index≥3), και η ουδετεροπενία (<500 πολυμορφοπύρηνα/mm3).
α. Εμπειρική αντιβιοτική θεραπεία στις σχετιζόμενες με την κοινότητα βακτηριαιμίες
Στις σχετιζόμενες με την κοινότητα βακτηριαιμίες, όπου τα πιθανότερα παθογόνα είναι ο Streptococcus pneumonia, ο Staphylococcus aureus και το Escherichia coli, κατάλληλη εμπειρική αντιβιοτική θεραπεία αποτελεί η χορήγηση ενός β-λακταμικού αντιβιοτικού. Η δραστηριότητα των β λακταμικών έναντι αυτών των βακτηριδίων δεν έχει αλλάξει την τελευταία δεκαετία. Η θεραπευτική μας επιλογή πρέπει να διαφοροποιηθεί όταν υπάρχουν παράγοντες κινδύνου για λοιμώξη από το Extended Spectrum Beta-Lactamase (ESBL)-producing E. Coli και τον «αποκτώμενο» στην κοινότητα MRSA (community acquired MRSA). Αυξημένη φορεία με ESBL E. Coli παρατηρείται μετά από ταξίδι σε ενδημικές περιοχές (23% οι ταξιδιώτες έναντι 4% των μη ταξιδιωτών)45. Ο MRSA της κοινότητας δεν αποτελεί σημαντικό πρόβλημα για την Ευρώπη, δεδομένου ότι απομονώνεται σε < 1% των περιπτώσεων πνευμονίας κοινότητας46, ενώ συναντάται συχνότερα στην Αμερική (8-10% των περιπτώσεων)47. Γενικά, θα πρέπει να καλύπτεται σε βακτηριαιμία που συνοδεύει περιπτώσεις σοβαρής νεκρωτικής πνευμονίας με αιμόπτυση και λευκοπενία48.
β. Εμπειρική αντιβιοτική θεραπεία στις ενδονοσοκομειακές και τις σχετιζόμενες με το σύστημα φροντίδας υγείας βακτηριαιμίες
β1. Εμπειρική αντιβιοτική θεραπεία για Gram- βακτηριαιμία
Η βιβλιογραφία δεν υποστηρίζει για την Gram- βακτηριαιμίατη χρήση της συνδυασμένης αντιμικροβιακής θεραπείας ως ρουτίνα49,50 εφόσον φυσικά η μονοθεραπεία είναι επαρκής51,52. Θεωρείται ότι δεν μειώνει τον κίνδυνο θανάτου, ενώ αντίθετα αυξάνει τον κίνδυνο επιπλοκών50,ακόμη και στις περιπτώσεις όπου η λοίμωξη από Pseudomonas Aeruginosa είναι ισχυρά ύποπτη51,52.Υπάρχουν, βέβαια, μελέτες53-55 που θεωρούν ότι σε ασθενείς με σοβαρή σήψη ή σηπτικό shock, με ουδετεροπενία ή με λοίμωξη από ανθεκτικά μικρόβια θα πρέπει να χρησιμοποιείται η συνδυασμένη εμπειρική θεραπεία. Η τελευταία σχετίστηκε με καταλληλότερη αντιβιοτική θεραπεία53,54 ή με βελτίωση της κλινικής απάντησης και της επιβίωσης σε αυτές τις κατηγορίες ασθενών55. Οι τελευταίες κατευθυντήριες οδηγίες για την σήψη και το σηπτικό shock56,πάντως, δεν συστήνουν την συνδυασμένη εμπειρική αντιβιοτική θεραπεία, ως ρουτίνα, για τις σοβαρές λοιμώξεις, συμπεριλαμβανομένων των βακτηριαιμιών και της σήψης, όταν αυτές δεν συνδυάζονται με shock (weak recommendation, low quality of evidence). Επίσης, δεν προτείνουν συνδυασμένη θεραπεία, ως ρουτίνα, στους ουδετεροπενικούς ασθενείς με σήψη/ βακτηριαιμία (strong recommendation, moderate quality of evidence). Οι ίδιες οδηγίες, όμως, υποστηρίζουν την χρήση συνδυασμένης εμπειρικής αντιβιοτικής θεραπείας για την αρχική αντιμετώπιση του σηπτικού shock (χρήση τουλάχιστον δύο αντιβιοτικών από διαφορετικές κατηγορίες αντιβιοτικών) στοχεύοντας στα πιο πιθανά παθογόνα (weak recommendation, low quality of evidence).
Σε ότι αφορά πάντως την αντιμετώπιση των ενδονοσοκομειακών λοιμώξεων αιματικής ροής από gram αρνητικά μικρόβια, τα βασικά θεραπευτικά διλλήματα στην επιλογή της εμπειρικής θεραπευτικής αγωγής προκύπτουν κυρίως, αν με βάση την τοπική επιδημιολογία, έχουμε αυξημένη:
- την παρουσία των ESBL – Εντεροβακτηριοειδών (E . coli, K. Pneumoniae & Proteus mirabilis)
- την αντίσταση των ESBL στις καρβαπενέμες, με κύριο εκπρόσωποτην παρουσία της Klebsiella που παράγει καρβαπενεμάση (Produced Carbapenemase Klebsiella – KPC)
- την παρουσία πολυανθεκτικού Acinetobacter baumannii
- την παρουσία πολυανθεκτικής Pseudomonas aeruginosa
- την αντίσταση στην κολιμυκίνη
ESBL – εντεροβακτηριοειδή
Για την αντιμετώπιση των λοιμώξεων από ESBL – εντεροβακτηριοειδή η αντίσταση στις 3ης γενιάς κεφαλοσπορίνες θα πρέπει να θεωρείται δεδομένη. Αυτό είναι ιδιαίτερα σημαντικό, καθώς οι Tumbarello et al57 έδειξαν ότι σε 186 ασθενείς με ESBL-βακτηριαιμίες, η ανεπαρκής αντιβιοτική θεραπεία, εντός 72 ωρών από την λήψη των αιμοκαλλιεργειών, οδήγησε σε 3πλάσια αύξηση της θνητότητας. Έτσι, οι καρβαπενέμες, με εξαίρεση την ερταπενέμη58,59, αποτελούν συνήθως την πρώτη επιλογή για την αντιμετώπιση αυτών των λοιμώξεων, ειδικά σε σοβαρά πάσχοντες ασθενείς με σηπτικό shock60.Σωστή εναλλακτική θεραπευτική επιλογή αποτελούν τα β-λακταμικά με αναστολέα της β-λακταμάσης (b lactam and b lactamase inhibitor, BLBLIs) προκειμένου να αποφευχθεί η αύξηση της αντίστασης στις καρβαπενέμες και η ανάπτυξη των εντεροβακτηριοειδών που παράγουν καρβαπενεμάση (carbapenemase-producing Enterobacteriacae (CRE). Προοπτικά cohort δεδομένα και μετα-αναλύσεις έδειξαν ότι τα BLBLIs, όπως η πιπερακιλλίνη/ταζομπακτάμη, δεν είναι κατώτερα από τις καρβαπενέμες για την θεραπεία αυτών των μικροβιαιμιών61 εφόσον χρησιμοποιούνται στη σωστή δοσολογία60,62,63.
Λοιμώξεις από Εντεροβακτηριοειδή που παράγουν καρβαπενεμάση – από KPC
Οι λοιμώξεις από εντεροβακτηριοειδή που παράγουν καρβαπενεμάση, και ειδικά από KPC, είναι σοβαρές λοιμώξεις με υψηλή θνητότητα ακόμη και στις περιπτώσεις που έλαβαν δραστική θεραπεία64. Οι Kontopidou et al64 σε πρόσφατη μελέτη 127 επεισοδίων KPC λοιμώξεων, μεταξύ των οποίων συμπεριλαμβάνονταν και πρωτοπαθείς βακτηριαιμίες (23.6%) ή βακτηριαιμίες από ΚΦΚ (30.7%), διαπίστωσαν ότι η θνητότητα στις 14 μέρες στο 45.2% των περιπτώσεων που έλαβαν δραστική θεραπεία ήταν 23.5%. Παρόλο αυτά, στην παραπάνω μελέτη, όσοι έλαβαν δραστική συνδυασμένη θεραπεία είχαν χαμηλότερη θνητότητα συγκριτικά με αυτούς που έλαβαν μονοθεραπεία ή ακατάλληλη θεραπεία. Για τις βακτηριαιμίες από KPC η βιβλιογραφία υποστηρίζει ισχυρά την συνδυασμένη αντιβιοτική θεραπεία έναντι της μονοθεραπείας, καθώς υπάρχει ξεκάθαρο όφελος τόσο στην θνητότητα65-68 όσο και στην θνητότητα από την λοίμωξη αυτή καθαυτή69 (Εικόνα 7). Οι πιο συχνά χρησιμοποιούμενοι συνδυασμοί περιλαμβάνουν τηνκολιμυκίνη ή την τιγεκυκλίνη με καρβαπενέμη70-73.Θεωρείται ότι, ειδικά η χρήση της κολιμυκίνης 64,72,74 στο αντιβιοτικό σχήμα βελτιώνει την κλινική ανταπόκριση. Θα πρέπει να ληφθεί σοβαρά υπόψη ότι οι συνδυασμοί αντιβιοτικών που περιείχαν την μεροπενέμη σχετίζονταν με σημαντικά υψηλότερα ποσοστά επιβίωσης όταν η KPC είχε MIC ≤8mg/L στην καρβαπενέμη66. Σε περιπτώσεις λοιμώξεων από KPC με υψηλή MIC στην καρβαπενέμη (μεροπενέμη MIC >8-16 mg/Ml) ή με αντίσταση στην κολιμυκίνη, υπάρχουν δεδομένα ότι ο συνδυασμός δύο καρβαπενεμών (ερταπενέμη με υψηλή δόση μεροπενέμης ή δοριπενέμης) μπορεί να είναι αποτελεσματικός75-77.
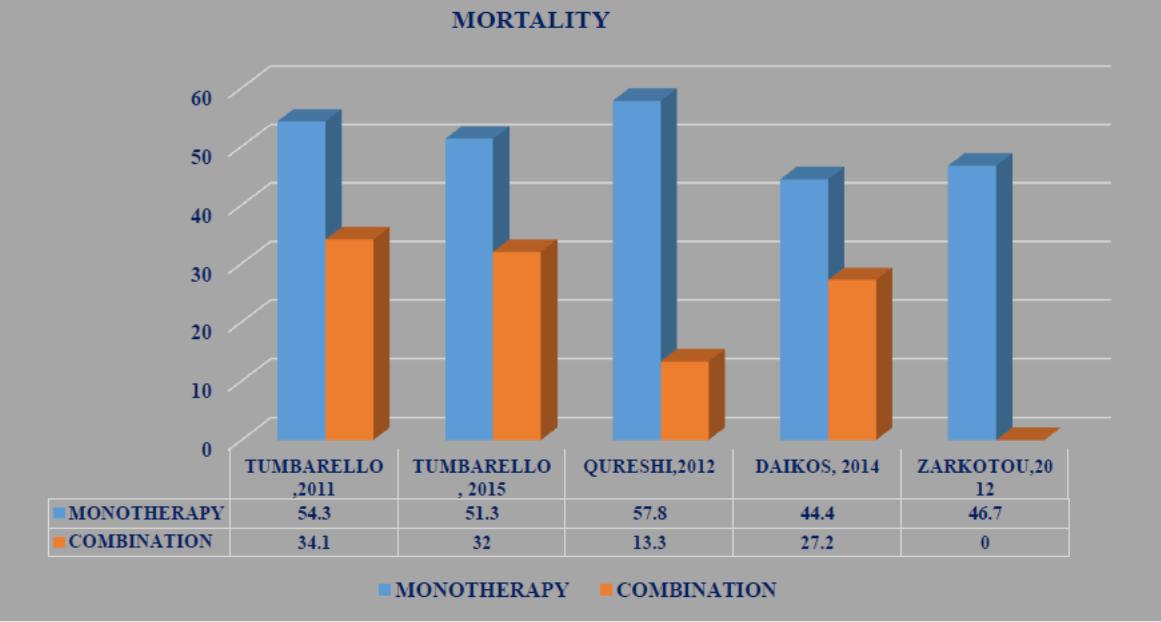
Εικόνα 7. Θνητότητα [δεδομένα από βιβλιογραφικές αναφορές 65: Tumbarello M et al (2012), 66: : Tumbarello M et al (2015), 67: Qureshi ΖΑ et al (2012), 68: Daikos GL et al (2014), 69: Zarkotou O et al (2011)].
Πολυανθεκτικό Acinetobacter baumannii
Δεν υπάρχει ξεκάθαρη σύσταση στην βιβλιογραφία σχετικά με το αν θα πρέπει να εφαρμόζεται μονοθεραπεία ή συνδυασμένη αντιβιοτική θεραπεία για την αντιμετώπιση των λοιμώξεων από MDRA cinetobacter baumannii (Αb)78. Οι καρβαπενέμες (εκτός από την ερταπενέμη) αν και αποτελούν το φάρμακο εκλογής για την θεραπεία του Αb, δεν θα πρέπει να χρησιμοποιούνται ως μονοθεραπεία σε περιοχές με υψηλά ποσοστά αντίστασης σε αυτά τα αντιβιοτικά. Ο συνδυασμός τους με σουλμπακτάμη, αμινογλυκοσίδες, πολυμυξίνες και τιγεκυκλίνη αποτελούν σωστές εμπειρικές θεραπευτικές επιλογές όταν υποψιαζόμαστε λοίμωξη από MDR/XDR/PDR Αb.
Σε ανθεκτικότητα στις καρβαπενέμες, η κολιμυκίνη έχει την καλύτερη in vitro δραστηριότητα και είναι το πιο ευρέως χρησιμοποιούμενο αντιβιοτικό έναντι του Αb. Συνηθέστερα συνδυάζεται με καρβαπενέμη, τιγεκυκλίνη. Σε συγκριτική μελέτη 250 ασθενών με BSI από XDR-Ab79 φάνηκε ότι η επιβίωση 14 ημερών, η εκρίζωση της λοίμωξης, και η ενδονοσοκομειακή θνητότητα ήταν σημαντικά καλύτερη στις ομάδες των ασθενών που έλαβαν συνδυασμένη θεραπεία σε σύγκριση με την ομάδα που έλαβε μονοθεραπεία. Ο συνδυασμός της κολιμυκίνης με ριφαμπικίνη έχει δείξει υψηλότερα ποσοστά εκρίζωσης της λοίμωξης σε σχέση με την μονοθεραπεία, χωρίς όμως καμιά επίδραση στην θνητότητα80. Τέλος, η συνδυασμένη θεραπεία κολιμυκίνης- γλυκοπεπτιδίου και κολιμυκίνης-φωσφομυκίνης φαίνεται να έχει συνεργική δράση έναντι του MDR Αb81,82.
Πολυανθεκτική Pseudomonas aeruginosa
Αν και βιβλιογραφικά δεν τεκμηριώνεται κάποιο όφελος στην επιβίωση με την συνδυασμένη αντιβιοτική θεραπεία για την πολυανθεκτική Pseudomonas aeruginosa51,52, ωστόσο προτείνεται ως ασφαλέστερη, τουλάχιστον κατά τις πρώτες 3-5 μέρες της λοίμωξης, και ενώ αναμένονται τα μικροβιολογικά αποτελέσματα78. Ιδανικός θεωρείται ο συνδυασμός ενός β-λακταμικού με αντιψευδομοναδική δράση (πιπερακιλλίνη/ταζομπακτάμη, κεφταζιδίμη ή καρβαπενέμη) με αμινογλυκοσίδη83.
Αντίσταση στην κολιμυκίνη
Μεγάλο πρόβλημα στη θεραπεία των βακτηριαιμιών από πολυανθεκτικά gram- βακτήρια φαίνεται να αποτελεί η αναδυόμενη αύξηση της αντίστασης στην κολιμυκίνη. Το φαινόμενο αυτό, ειδικά για την Klebsiella pneumoniae (Colimycin Resistant Klebsiella Pneumoniae, CoRKP), σε αρκετές χώρες παγκοσμίως, συμπεριλαμβανομένης και της Ευρώπης, φαίνεται να έχει πάρει ανησυχητικές διαστάσεις. Πράγματι οι Parisi et al84 σε μελέτη 15000 περίπου ασθενών διαπίστωσαν ότι, στην διάρκεια μιας τριετίας, υπήρχε μια στατιστικά σημαντική αύξηση της απομόνωσης KPC από κλινικά δείγματα και από καλλιέργειες επιτήρησης σε δείγματα πρωκτού (p<0.001). Το πιο αξιοσημείωτο στην παραπάνω μελέτη ήταν η αύξηση, κατά τρόπο στατιστικά σημαντικό, της αντίστασης στην κολιμυκίνη των στελεχών KPC στη διάρκεια των δύο χρονικών περιόδων μελέτης (p=0.0019 μεταξύ 2012-2013 και p=0.008 για τα έτη 2013-2014). Τούτο φαίνεται να οφείλεται στη συνεχή χρήση της κολιμυκίνης για τα MDR gram- βακτήρια. Τα ποσοστά αντίστασης μάλιστα συνεχώς αυξάνονται, και ειδικά στην Ελλάδα φτάνουν στο 20%.
Διάφοροι συνδυασμοί φαρμάκων, που κυρίως είναι βασισμένοι στην κολιμυκίνη, συνδέονται με επιτυχή αντιμετώπιση των λοιμώξεων αυτών74. Υποσχόμενοι, ειδικά για τις λοιμώξεις από την PDR Klebsiella, είναι οι συνδυασμοί με τιγεκυκλίνη σε μεγάλες δόσεις85, με μεροπενέμη86και φωσφομυκίνη . Η φωσφομυκίνη φαίνεται επίσης να έχει δραστηριότητα έναντι των Gram αρνητικών βακτηριδίων που παράγουν καρβαπενεμάση και ειδικά για τις λοιμώξεις από CoRKP. Ο συνδυασμός της με τιγεκυκλίνη ή κολιμυκίνη87 και με μεροπενέμη88, σχετίστηκε με θεραπευτική επιτυχία. Επίσης, η χορήγηση της με καρβαπενέμες και αμινογλυκοσίδες (ειδικά γενταμυκίνη) είχε καλά αποτελέσματα60,68.
Συμπερασματικά, σε ότι αφορά την εμπειρική αντιβιοτική θεραπεία για Gram- βακτηριαιμία σε βαρέως πάσχοντες ασθενείς, που παρουσιάζονται με σοβαρή σήψη ή σηπτικό shock, και έχουμε αυξημένη υποψία λοίμωξης από ανθεκτικό στην καρβαπενέμη μικροοργανισμό θα πρέπει να μελετάται η κάλυψη του ασθενούς με τον συνδυασμό μεροπενέμης (1-2gr/6-8h), κολιμυκίνης (9×106/d) και τιγεκυκλίνης (200mg/d)16. Η υποψία τίθεται από προηγούμενο αποικισμό του ασθενούς, προηγηθείσα λοίμωξη με ανθεκτικό στην καρβαπενέμη στέλεχος ή βάσει της τοπικής επιδημιολογίας.
β2. Εμπειρική αντιβιοτική θεραπεία για Gram+ βακτηριαιμία
Σε βαρέως πάσχοντα ασθενή με ύποπτη βακτηριαιμία, όπου επιβάλλεται η εμπειρική κάλυψη για gram θετικά βακτήρια βάσει τοπικής επιδημιολογίας, ποστηρίζεται η χρήση της βανκομυκίνης (Α-ΙΙ) ή της δαπτομυκίνης (Α-Ι)89. Η δαπτομυκίνη, με την ταχεία βακτηριοκτόνο δράση της, φαίνεται ότι αποτελεί καλή εναλλακτική λύση για τα προβλήματα που ανακύπτουν από το “MIC–creep” φαινόμενο για τον MRSA. Έχει καλή δράση έναντι του vancomycin hetero-resistant S. aureus (h-VISA) (MIC 1-4 mg/mL), vancomycin-intermediate S. aureus (VISA) (MIC 8-16 mg/mL),vancomycin-resistant S. aureus (VRSA) (MIC>32 mg/mL).Εξάλλου, βιβλιογραφικά δεδομένα υποστηρίζουν ότι σε παρουσία MRSA με MIC στην βανκομυκίνη >1 mg/L, η θεραπεία με βανκομυκίνη έχει συσχετισθεί με κλινική αποτυχία και υψηλότερη θνητότητα 30 ημερών συγκριτικά με την δαπτομυκίνη89-91. Επιπλέον, η δαπτομυκίνη έχει και καλή δράση έναντι των biofilm, κάτι ιδιαίτερα σημαντικό σε βακτηριαιμία από ΚΦΚ92. Έτσι, σε ύποπτη MRSA βακτηριαιμία, ειδικά όταν η τοπική επιδημιολογία αναδεικνύει υψηλή επίπτωση MRSA, υψηλή δόση δαπτομυκίνης (8-10 mg/kg/μέρα) αποτελεί καλύτερη εμπειρική θεραπευτική επιλογή έναντι επαρκούς δόσης ενός γλυκοπεπτιδίου93.
ΙΙ. ΔΟΣΟΛΟΓΙΑ
Στο πλαίσιο της κατάλληλης και αποτελεσματικής αντιβιοτικής θεραπείας εντάσσεται και η χορήγηση της στη σωστή δοσολογία και οδό. Αυτό έχει μεγάλη σημασία ειδικά για τους βαρέως πάσχοντες ασθενείς, που πιθανότατα έχουν αυξημένο όγκο κατανομής των αντιβιοτικών, και για τα παθογόνα, που με βάση την MIC τους, είναι οριακά ευαίσθητα στα διαθέσιμα αντιμικροβιακά. Προκειμένου να επιτευχθεί η σωστή δοσολογία θα πρέπει να λαμβάνονται υπόψη τα στοιχεία φαρμακοκινητικής και φαρμακοδυναμικής των επιλεγμένων φαρμάκων. Έτσι μειώνεται ο κίνδυνος κλινικής αποτυχίας αλλά και ο κίνδυνος αύξησης της μικροβιακής αντίστασης.
Μετά την επιλογή του κατάλληλου αντιβιοτικού, βασικό είναι να γνωρίζουμε αρχικά αν αυτό είναι χρονο-εξαρτώμενο (time-dependent) ή εξαρτώμενο από την συγκέντρωση (concentration-dependent), καθώς και αν είναι υδρόφιλο ή λιπόφιλο. Για τα time-dependent αντιβιοτκά (β-λακτάμες-γλυκοπεπτίδια) θα πρέπει να προτιμάται η παρατεταμένη ή συνεχής χορήγηση, ενώ για τα concentration- dependent (αμινογλυκοσίδες-κολιμυκίνη) συστήνεται η αύξηση της δοσολογίας τους, ώστε να επιτευχθούν οι φαρμακοδυναμικοί στόχοι. Για τα υδρόφιλα αντιβιοτικά, όπως β-λακτάμες, αμινογλυκοσίδες, γλυκοπεπτίδια, ή κολιμυκίνη θα πρέπει να ληφθεί υπόψη ότι, η αύξηση του όγκου κατανομής που παρατηρείται στους βαρέως πάσχοντες ασθενείς, ενδεχομένως, θα μειώσει την συγκέντρωση των παραπάνω αντιβιοτικών. Αντίθετα, ο όγκος κατανομής των λιπόφιλων αντιβιοτικών, όπως οι φθοριοκινολόνες, είναι αμετάβλητος ενώ η κάθαρση τους εξαρτάται από την ηπατική λειτουργία. Θα πρέπει να λαμβάνεται, επίσης, σοβαρά υπόψη αν η νεφρική λειτουργία του ασθενούς υποστηρίζεται με συνεχή φλεβο-φλεβική αιμοδιαδιήθηση, διότι επιφέρει σημαντικές μεταβολές στην τελική συγκέντρωση του φαρμάκου. Τέλος, βασικό είναι να γνωρίζουμε τον χρόνο πάνω από την MIC για τις β-λακτάμες, καρβαπενέμες, και τον λόγο της μέγιστης συγκέντρωσης (Cmax) προς την MIC (Cmax / MIC) για τις κινολόνες, τις αμινογλυκοσίδες, την δαπτομυκίνη και την κολιμυκίνη. Για τα γλυκοπεπτίδια είναι σημαντική η περιοχή κάτω από την καμπύλη που είναι πάνω από την MIC (AUIC). Για τα β-λακταμικά υψηλής σημασίας είναι η ελεύθερη συγκέντρωση του αντιβιοτικού πάνω από την MIC του παθογόνου (fT > MIC) στο 50 και 100% του διαστήματος χορήγησης τους.
Οι προτεινόμενες δοσολογίες ανά τάξη αντιβιοτικών φαίνεται στον πίνακα 1.
Πίνακας 1. Δοσολογία ανά τάξη αντιβιοτικών.
| Κατηγορία αντιβιοτικών | |
| Αμινογλυκοσίδες* | Αμικασίνη 25mg/Kg-1
Γενταμυκίνη 7mg/Kg-1 |
| Φθοροκινολόνες | Σιπροφλοξασίνη 400mg/8h |
| Κολιστίνη | Δόση φόρτισης: 9-12 MU (720-960mg),
Δόση συντήρησης:480mg/12h (χωρίς νεφρική βλάβη) |
| Β-λακτάμες | Κεφεπίμη 2gr/8h
Κεφταδιζίμη 2gr/6h Ιμιπενέμη 1gr/6-8h Μεροπενέμη 1gr/6-8h Ερταπενέμη 1gr/12h Πιπερακιλλίνη-Ταζομπακτάμη 4.5gr/8h |
| Γλυκοπεπτίδια | Βανκομυκίμη 35mg/kg ως δόση φόρτισης σε 1h ακολουθούμενη από 30mg/kg συνεχούς έγχυσης. |
| Δαπτομυκίνη | 8-12 mg/Kg/24h |
| Τιγεκυκλίνη | 200 ακολουθούμενα από 100/12 σε υποψία οριακής ευαισθησίας |
ΙΙΙ. ΣΤΟΧΕΥΜΕΝΗ ΘΕΡΑΠΕΙΑ
Μετά την λήψη των test ευαισθησίας από τις καλλιέργειες πρέπει να εφαρμόζεται η στοχευμένη θεραπεία. Βάσει βιβλιογραφικών δεδομένων στο 20-40 % η εμπειρική αντιβιοτική θεραπεία παραμένει ανεπαρκής12. Η στοχευμένη θεραπεία ουσιαστικά συνίσταται στον επανακαθορισμό της αντιβιοτικής αγωγής, στην εφαρμογή της αποκλιμάκωσης (de-escalation) και στον καθορισμό της διάρκειας της θεραπείας.
α. Επανακαθορισμός αντιβιοτικής αγωγής
Μετά την λήψη του αντιβιογράμματος και του test ευαισθησίας του απομονωθέντος μικροοργανισμού καθορίζεται οριστικά το ιδανικό αντιβιοτικό σχήμα. Υπάρχουν κάποια ειδικά σημεία που πρέπει να έχουμε υπόψη κατά την θεραπεία των δύσκολων στην αντιμετώπιση λοιμώξεων.
Gram – βακτηριαιμία
Για την θεραπεία της Gram – βακτηριαιμίας ισχύουν όλα όσα αναφέρθηκαν στην εμπειρική θεραπεία με τις εξής ιδιαίτερες επισημάνσεις:
ESBL – εντεροβακτηριοειδή
Η χρήση των καρβαπενεμών πρέπει να διαφυλαχτεί για τις σοβαρές λοιμώξεις από ESBL – εντεροβακτηριοειδή ενώ τα BLBLIs αποτελούν την καλύτερη εναλλακτική λύση σε σταθερούς ασθενείς ειδικά όταν η MIC για την πιπερακιλλίνη/ταζομπακτάμη είναι ≤16/4 mg/mL. Παρότι υπάρχει μικρή κλινική εμπειρία για να προταθεί η χρήση αντιβιοτικών από άλλες τάξεις (όπως τιγεκυκλίνη, αμινογλυκοσίδες, φωσφομυκίνη, φθοριοκινολόνες, ή τριμεθοπρίμη/ σουλφομεθοξαζόλη), ωστόσο θα μπορούσαν να αποτελούν εναλλακτικές θεραπευτικές επιλογές βάσει των test ευαισθησίας78.
Λοιμώξεις από KPC
Σε KPC με MIC ≤8-16 mg/L στην μεροπενέμη προτείνεται η χρήση της σε υψηλές δόσεις και σε παρατεταμένη έγχυση σε συνδυαστικό σχήμα (με άλλα δύο αντιβιοτικά που έχουν in vitro ευαισθησία). Όταν η MIC είναι > 16 mg/L οι καρβαπενέμες πρέπει να εξαιρούνται από το συνδυαστικό αντιβιοτικό σχήμα, το οποίο πρέπει να καθορίζεται με βάση την in vitro ευαισθησία. Ο συνδυασμός δύο καρβαπενεμών μπορεί να είναι αποτελεσματικός σε περιπτώσεις με αντίσταση στην κολιμυκίνη ή σε υψηλή MIC στην μεροπενέμη >8-16 mg/L78.
Πολυανθεκτικό Acinetobacter baumannii
Ο συνδυασμός της σουλβακτάμης ή κολιμυκίνης με έναν δεύτερο αντιμικροβιακό παράγοντα (τιγεκυκλίνη, ριφαμπικίνη ή φωσφομυκίνη) θα πρέπει να μελετάται σε κλινική αποτυχία ή σε σε περίπτωση που ο μικροοργανισμός έχει MIC στα ανώτερα όρια της ευαισθησίας78. Ένα πιθανό όφελος από τη συνδυασμένη θεραπεία είναι η πρόληψη της εμφάνισης αντοχής (ειδικά για την κολιμυκίνη και την τιγεκυκλίνη)94.
Πολυανθεκτική Pseudomonas aeruginosa
Σε περίπτωση απομόνωσηςPseudomonas aeruginosa, με βάση το test ευαισθησίας, προτείνεται η αποκλιμάκωση από την εμπειρική συνδυαστική αντιβιοτική θεραπεία σε μονοθεραπεία. Η κολιμυκίνη πρέπει να φυλάσσεται για την θεραπεία παθογόνων ανθεκτικών στα υπόλοιπα αντιβιοτικά.
Διαχείριση MRSA βακτηριαμίας
Βασικό κλινικό πρόβλημα αποτελεί η αντιμετώπιση της MRSA βακτηριαιμίας. Μείζονος σημασίας είναι η σωστή ερμηνεία του αντιβιογράμματος του στελέχους σε συνδυασμό με την κλινική απόκριση του ασθενούς89. Με βάση, λοιπόν, τις κατευθυντήριες οδηγίες89, για στέλεχος σταφυλοκόκκου με MIC στην βανκομυκίνη ≤ 2 μg/ml, η συνέχιση χορήγησης του φαρμάκου θα εξαρτηθεί αποκλειστικά και μόνο από την κλινική και μικροβιολογική απάντηση του ασθενούς. Εάν υπάρχει θετική απάντηση, προτείνεται η συνέχιση της θεραπείας, με στενή παρακολούθηση όλων των παραμέτρων. Σε επίμονη MRSA βακτηριαιμία, σε κλινική αποτυχία της βανκομυκίνης και σε στέλεχος σταφυλοκόκκου με MIC στην βανκομυκίνη >2 μg/ml (VISA, VRSA)89 θα πρέπει πρώτα να διερευνάται ενδελεχώς η περίπτωση παρουσίας άλλης εστίας λοίμωξης, η οποία θα πρέπει να απομακρύνεται άμεσα. Συγχρόνως, προτείνεται η χρήση της δαπτομυκίνης σε υψηλή δόση (10mg/Kg/ ημερησίως), σε συνδυασμό με γενταμυκίνη(1mg/kg IV/ 8h), ριφαμπικίνη (600 mg PO/IV ημερησίως ή 300-450 mg PO/IV δύο φορές την ημέρα), λινεζολίδη (600 mg PO/I δύο φορές την ημέρα) ή τριμεθοπρίμη-σουλφομεθοξαζόλη (5 mg/kg IV δύο φορές την ημέρα) ή ένα β λακταμικό αντιβιοτικό (B-III)89. Σε περίπτωση μειωμένης ευαισθησίας και στην δαπτομυκίνη και στην βανκομυκίνη οι θεραπευτικές επιλογές περιορίζονται στην quinupristin-dalfopristin (7.5 mg/kg IV / 8h), στην τριμεθοπρίμη-σουλφομεθοξαζόλη (5 mg/kg IV δύο φορές την ημέρα), στην λινεζολίδη (600 mg PO/I δύο φορές την ημέρα), ή τελαβανσίνη (10 mg/kg IV μία φορά την ημέρα) (C-III)89. Τα παραπάνω αντιβιοτικά χορηγούνται είτε ως μονοθεραπεία ή σε συνδυασμό με άλλης τάξης αντιβιοτικά.
β. Αποκλιμάκωση
Η αποκλιμάκωση, στην κλινική πράξη, εφαρμόζεται σε περίπου 50% των περιπτώσεων95 ακόμη κι όταν οι καλλιέργειες είναι διαθέσιμες. Η αποτελεσματικότητα της αποκλιμάκωσης στη μείωση της αντίστασης στα αντιβιοτικά και στην κατανάλωση των αντιβιοτικών δεν έχει αποδειχθεί ενώ αντικρουόμενα είναι τα δεδομένα για την επίδραση της στην θνητότητα96,97. Επίσης, δεν υπάρχουν ασφαλή συμπεράσματα για την επίδραση της στο ποσοστό των επαναλοιμώξεων και στη διάρκεια παραμονής στη ΜΕΘ, δεδομένου ότι απουσιάζουν μελέτες με εφαρμογή της σε σοβαρές λοιμώξεις από MDR/XDR παθογόνα. Ωστόσο, η βιβλιογραφία υποστηρίζει ότι η αποκλιμάκωση θα πρέπει να ενθαρρύνεται ως πρακτική με βάση το κλινικό κριτήριο12,16,56, με καθημερινή εκτίμηση της δυνατότητας εφαρμογής της56. Οι τελευταίες κατευθυντήριες οδηγίες56 συστήνουν την απόσυρση ενός ή περισσότερων αντιμικροβιακών φαρμάκων ή τη μετάβαση σε έναν αντιβιοτικό παράγοντα στενότερου φάσματος, εφόσον έχουν καθοριστεί οι ευαισθησίες του παθογόνου, όταν υπάρχει κλινική βελτίωση και σημεία ελέγχου της λοίμωξης.
Πιθανές στρατηγικές αποκλιμάκωσης αποτελούν η χρήση οξακιλλίνης για τον MSSA ή MSSE, η χρήση αμπικιλλίνης για τον ευαίσθητο enterococcusfaecalis, η χρήση κεφαλοσπορίνης γ΄γενιάς για τα ESBL εντεροβακτηριοειδή ή ερταπενέμης για τα non-ESBL εντεροβακτηριοειδή, η χρήση μιας αντιψευδομοναδικής κεφαλοσπορίνης για την ευαίσθητη P.aeruginosa.
γ. Διάρκεια θεραπείας
Η ιδανική διάρκεια θεραπείας των βακτηριαιμιών σε βαρέως πάσχοντες ασθενείς δεν έχει μελετηθεί και καθοριστεί σε μεγάλες τυχαιοποιημένες μελέτες16. Ωστόσο, η μείωση στην διάρκεια θεραπείας είναι μια σημαντική στρατηγική για την ελαχιστοποίηση των συνεπειών που προκύπτουν από την κατάχρηση των αντιβιοτικών, όπως η αναδυόμενη αντίσταση στα αντιβιοτικά, η σχετιζόμενη με το Clostridium Difficile διάρροια, οι ανεπιθύμητες ενέργειες από την χρήση κάθε φαρμάκου και το κόστος θεραπείας12. Οι Havey et al98 σε μια συστηματική ανασκόπηση και μετα-ανάλυση διαπίστωσαν ότι τα μικρής διάρκειας (5-7 ημερών) θεραπευτικά σχήματα συγκρινόμενα με τα μεγάλης διάρκειας (7-14 ημερών) στις βακτηριαιμίες δεν είχαν σημαντικές διαφορές στην κλινική ίαση, στην μικροβιολογική θεραπεία και στην επιβίωση. Οι Daneman et al99 προτείνουν θεραπευτικά σχήματα ≤ 10 ημερών για την βακτηριαιμία που σχετίζεται με ΚΦΚ, πνευμονία, λοιμώξεις ουροποιητικού, και ενδοκοιλιακές λοιμώξεις αλλά μεγαλύτερης διάρκεια θεραπεία (14μέρες ± 3.8) για βακτηριαιμία που σχετίζεται με λοιμώξεις δέρματος και μαλακών μορίων. Μεγαλύτερη επίσης διάρκεια θεραπείας προτείνουν για τον Staphylococcus aureus και μικρότερη για τους coagulase-αρνητικούς σταφυλόκοκκους. Ωστόσο, ορθότερη θεωρείται η πρακτική κατά την οποία η διάρκεια θεραπείας καθορίζεται βάσει παραγόντων που σχετίζονται με τον ασθενή, το είδος της λοίμωξης και τα φάρμακα που χορηγούνται. Έτσι, βραχείας διάρκειας θεραπευτικά σχήματα είναι ασφαλή κατά την αντιμετώπιση πλήρως ευαίσθητων μικροοργανισμών, χωρίς κίνδυνο αντίστασης στα αντιβιοτικά ή όταν χρησιμοποιούνται γρήγορης δράσης και βακτηριοκτόνα αντιβιοτικά στην ιδανική δόση ή σε ιδανικό θεραπευτικό σχήμα (π.χ. συνδυασμένη θεραπεία)100. Επίσης, ασφαλή θεωρούνται τα αντιμικροβιακά που είναι δραστικά έναντι μη διαιρούμενων βακτηριδίων και αυτά που έχουν καλή διείσδυση στην εστία λοίμωξης. Τέλος, η επιλογή μικρής διάρκειας θεραπείας είναι κατάλληλη σε απουσία ξένου σώματος, αποστήματος ή σημείων ανοσοανεπάρκειας100 ή σε ταχεία κλινική βελτίωση που ακολουθεί αποτελεσματικό έλεγχο ενδοκοιλιακής λοίμωξης, λοίμωξης ουροποιητκού ή ανατομικά ανεπίπλεκτης πυελονεφρίτιδας56.
Προκαλσιτονίνη
Τελευταία, στην βιβλιογραφία η προκαλσιτονίνη έχει αναγνωριστεί ως κατάλληλος δείκτης καθορισμού της διάρκειας της θεραπείας101,102. Η καθοδηγούμενη από την προκαλσιτονίνη διάρκεια θεραπείας συγκρινόμενη με την standard θεραπεία δεν είχε καμιά διαφορά στη νοσοκομειακή θνητότητα και στην θνητότητα 28 ημερών101 αλλά σχετιζόταν με μικρότερη μέση διάρκεια αντιμικροβιακής θεραπείας 101,102. Οι τελευταίες κατευθυντήριες οδηγίες για την σήψη και το σηπτικό shock56 προτείνουν ότι τα επίπεδα της προκαλσιτονίνης μπορούν να υποστηρίξουν την βράχυνση της διάρκειας του αντιμικροβιακού σχήματος στους σηπτικούς ασθενείς (weak recommendation, low quality of evidence), ή ακόμη και την διακοπή της αντιβιοτικής θεραπείας στους ασθενείς που δεν αποδείχτηκε λοίμωξη (weak recommendation, lowquality of evidence).
IV. ΕΛΕΓΧΟΣ ΕΣΤΙΑΣ ΛΟΙΜΩΞΗΣ
Αποτελεί σημαντικό μέρος της θεραπείας των βακτηριαιμιών, και μάλιστα συσχετίζεται ανεξάρτητα με την έκβαση14,103. Πράγματι στην μελέτη Eurobact14 η 28d θνητότητα ήταν σημαντικά μεγαλύτερη επί απουσίας ελέγχου της πηγής της βακτηριαιμίας (π.χ. απομάκρυνση ΚΦΚ, χειρουργικός έλεγχος ενδοκοιλιακής λοίμωξης) σε σύγκριση με την ομάδα που έγινε έλεγχος πηγής λοίμωξης(69.4 vs 30.6,p<0.0001). O έλεγχος της πηγής της λοίμωξης είναι ιδιαίτερα σημαντικός όταν οι υπεύθυνοι μικροοργανισμοί είναι λιγότερο ευαίσθητοι στα αντιβιοτικά ή όταν η διείσδυση των αντιβιοτικών δεν είναι βέβαιη. Ανάλογα με την εστία της λοίμωξης (Πνευμονία (CAP,HAP,VAP), ΚΦΚ, λοιμώξεις ουροποιητικού, ενδοκοιλιακές λοιμώξεις) η επιλογή της θεραπευτικής τακτικής πρέπει να βασίζεται στις διεθνείς κατευθυντήριες οδηγίες σε συνδυασμό πάντα με την τοπική μικροβιολογία και τα τοπικά δεδομένα αντίστασης στα αντιβιοτικά104-108.
Διαχείριση ασθενούς με περιφερικό φλεβικό καθετήρα
Οι περιφερικοί φλεβικοί καθετήρες που σχετίζονται με πόνο, σκληρία, ερύθημα ή εξοίδηση υγρού πρέπει να απομακρύνονται άμεσα (Α-Ι )15. Επίσης οποιαδήποτε εξοίδηση στο σημείο εισόδου του καθετήρα πρέπει να αποστέλλεται για Gram χρώση, καλλιέργεια και επιπρόσθετη καλλιέργεια για μύκητες και οξεάντοχους οργανισμούς ειδικά σε ανοσοκατεσταλμένους (Α-ΙΙ)15.
Διαχείριση ασθενούς με κεντρικό φλεβικό ή αρτηριακό καθετήρα
Σε ασθενής με ΚΦΚ ή αρτηριακό καθετήρα (ΑΚ) και οξύ εμπύρετο επεισόδιο, εφόσον συνοδεύεται από βαριά κλινική εικόνα (υπόταση, υπό-άρδευση, MOF) συνιστάται λήψη δύο ζευγών αιμοκαλλιεργειών με σύγχρονη απομάκρυνση του ΚΦΚ και του ΑΚ, καλλιέργεια του άκρου αυτών, και τοποθέτηση νέου ΚΦΚ και ΑΚ σε νέα θέση με έναρξη κατάλληλης αντιμικροβιακής θεραπείας15,56. Εφόσον στοιχειοθετείται λοίμωξη αιματικής ροής από ΚΦΚ, έχει σημασία η διάκριση αυτής σε επιπλεγμένη ή μη λοίμωξη.
- Ως μη επιπλεγμένη θεωρείται η λοίμωξη όπου έχουμε λύση του πυρετού σε 72 ώρες, και ο ασθενής δεν έχει ενδαγγειακή συσκευή, δεν έχει στοιχεία ενδοκαρδίτιδας ή διαπυητικής θρομβοφλεβίτιδας, ενεργού κακοήθειας ή ανοσοκαταστολής. Η διάρκεια της θεραπείας καθορίζεται από το είδος του μικροοργανισμού που απομονώθηκε. Για τους κοαγκουλάση(-)σταφυλοκόκκους προτείνεται συστηματική χορήγηση αντιβιοτικών για 5-7 μέρες, ενώ για τον staphylococcusaureus για ≥ 14 μέρες, και για τον εντερόκοκκο και τα gram αρνητικά βακτήρια 7- 14 μέρες15.
- Σε επιπλεγμένη λοίμωξη, δηλαδή σε παρουσία διαπυητικής θρομβοφλεβίτιδας, ενδοκαρδίτιδας προτείνεται συστηματική χορήγηση αντιβιοτικών για 4-6 εβδομάδες ενώ επί παρουσίας οστεομυελίτιδας για 6-8 εβδομάδες15.
Διαχείριση ασθενούς με tunneled καθετήρες αιμοδιάλυσης
Σε ασθενή με tunneled καθετήρες αιμοδιάλυσης και ύποπτη βακτηριαιμία, συνιστάται η λήψη καλλιεργειών από τον καθετήρα και μια περιφερική φλέβα και η εφαρμογή εμπειρικής αντιβιοτικής θεραπείας με ενδοαυλική παγίδευση αντιβιοτικού (Antibiotic Lock Therapy).
- Επί αρνητικών αιμοκαλλιεργειών, συνιστάται διακοπή των αντιβιοτικών.
- Σε λύση της βακτηριαιμίας και του πυρετού σε 2-3 μέρες και απομόνωση κοαγκουλάση (-) σταφυλοκόκκωνή Gram αρνητικών βακτηρίων, συνιστάται διατήρηση του καθετήρα και συστηματικά αντιβιοτικά για 5-7ημέρες με συνέχιση της ενδοαυλικής παγίδευσης αντιβιοτικού ή αλλαγή του καθετήρα με σύρμα.
- Επί απομόνωσηςχρυσίζοντα σταφυλόκοκου, συνιστάται απομάκρυνση του καθετήρα και συστηματική χορήγηση αντιβιοτικών για 3 εβδομάδες εφόσον το διοισαφάγειο υπερηχογράφημα καρδιάς είναι αρνητικό.
- Σε επίμονη βακτηριαιμία και πυρετό, προτείνεται η απομάκρυνση του καθετήρα, η χορήγηση αντιβιοτικών για 4-6 εβδομάδες και ο έλεγχος για μεταστατική λοίμωξη (θρόμβωση,ενδοκαρδίτιδα).
Διαχείριση ασθενούς με long-term ΚΦΚ ή Port
- Σε μη επιπλεγμένη βακτηριαιμία που σχετίζεται με long-term ΚΦΚ ή Port (Ρ)και απομόνωση κοαγκουλάση(-)σταφυλοκόκκων και εντεροκόκκων συνιστάται η διατήρηση του ΚΦΚ/Ρ μαζί με συστηματικά αντιβιοτικά και antibiotic lock θεραπεία για 10-14 ή 7-14 ημέρες, αντίστοιχα.
- Για μη επιπλεγμένη βακτηριαιμία long-term ΚΦΚ/Ρ από Gram αρνητικά βακτήρια προτείνεται η απομάκρυνση του ΚΦΚ/Ρ μαζί με συστηματική χορήγηση αντιβιοτικών για 7-14 μέρες ενώ για διάσωση του ΚΦΚ/Ρ συστηματική χορήγηση αντιβιοτικών με antibiotic lock θεραπεία για 10-14 μέρες.
Αν δεν υπάρχει απάντηση σε όλες τις παραπάνω καταστάσεις συνιστάται η απομάκρυνση του καθετήρα, σύγχρονος έλεγχος για ενδοκαρδίτιδα ή διαπυητική θρομβοφλεβίτιδα με συστηματική χορήγηση αντιβιοτικών για 10-14 μέρες.
- Σε απομόνωση staphylococcusaureus συνιστάται η απομάκρυνση του καθετήρα και χορήγηση συστηματικών αντιβιοτικών για 4-6 εβδομάδες εκτός εξαιρέσεων (παρουσία ανοσοκαταστολής, σακχαρώδους διαβήτη, πρόσθετης ενδοαγγειακής συσκευής, παρουσία ενδοκαρδίτιδας ή θρομβοφλεβίτιδας ή μεταστατικής λοίμωξης).
- Σε επιπλεγμένη λοίμωξη ή με παρουσία αποστήματος του port απαιτείται η απομάκρυνση του καθετήρα ή portκαι συστηματικά αντιβιοτικά για 7-10 ημέρες.
- Σε σηπτική θρόμβωση ή ενδοκαρδίτιδα επιβάλλεται η απομάκρυνση καθετήρα και θεραπεία για 4-6 εβδομάδες ενώ σε παρουσία οστεομυελίτιδας παράταση της συστηματικής αντιβιοτικής θεραπείας για 6-8 εβδομάδες σε ενήλικες.
Συμπέρασμα
Το κλειδί για την καλύτερη έκβαση των βακτηριαιμιών, ειδικά από MDR παθογόνα, αποτελεί η πρώιμη έναρξη της αποτελεσματικότερης αντιβιοτικής θεραπείας, προσαρμοσμένη σε κάθε ασθενή με βάση την εστία της λοίμωξης, τα πιο κοινά παθογόνα (σύμφωνα με την τοπική επιδημιολογία) και την αντίσταση στα αντιβιοτικά109. Σήμερα, ωστόσο, παρατηρείται μια ολοένα αυξανόμενηχρήση των ευρέως φάσματος αντιβιοτικών στην εμπειρική αντιβιοτική αγωγή, ειδικά σε ασθενείς με σοβαρά υποκείμενα νοσήματα και ανοσοκαταστολή, προκειμένου αυτή να είναι αποτελεσματική. Αυτόόμως επιδεινώνει τον φαύλο κύκλο της δημιουργίας ανθεκτικών στελεχών, περιορίζοντας τις θεραπευτικές μας επιλογές, ειδικά για σοβαρές λοιμώξεις. Τούτο λαμβάνει ακόμη πιο ανησυχητικές διαστάσεις αν λάβουμε υπόψη ότι την τελευταία δεκαετία δεν έχουν προστεθεί νέοι παράγοντες στην αντιμικροβιακή θεραπεία. Η γρήγορη διάγνωση και πρώιμη ανίχνευση του υπεύθυνου μικροοργανισμού ίσως αποτελεί μια λύση στο πρόβλημα, δημιουργώντας προοπτικές για στοχευμένες θεραπείες στενότερου φάσματος στα πρώιμα στάδια της λοίμωξης. Επίσης, στρατηγικές όπως προσεχτική διαχείριση των διαθέσιμων ευρέως φάσματος αντιμικροβιακών, βάσει τοπικής επιδημιολογίας, και βελτίωση των προγραμμάτων επιτήρησης και πρόληψης λοιμώξεων, όπως αυτά που αφορούν την τοποθέτηση και διαχείριση των ΚΦΚ, παίζουν σημαντικό ρόλο στο σχεδιασμό πολιτικών ορθής αντιμετώπισης των βακτηριαιμιών.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Timsit JF, Laupland KB: Update on bloodstream infections in ICUs. Curr Opin Crit Care 2012;18:479–86.
- Prowle JR, Echeverri JE, Ligabo EV, et al. Acquired bloodstream infection in the intensive care unit: Incidence and attributable mortality. Crit Care 2011; 15:R100.
- Soufir L, Timsit JF, Mahe C, et al. Attributable morbidity and mortality of catheterrelated septicemia in critically ill patients: A matched, risk-adjusted, cohort study. Infect Control Hosp Epidemiol 1999; 20:396-401.
- Gahlot R, Nigam C, Kumar V, et al. Catheter-related bloodstream infections. Int J Crit Illn Inj Sci 2014; 4:162-7.
- O’Horo JC, Maki DG, Krupp AE, et al. Arterial catheters as a source of bloodstream infection: A systematic review and meta-analysis. Crit Care Med 2014; 42:1334-9.
- Magill SS, Edwards JR, Bamberg W, et al. Emerging Infections Program Healthcare-Associated Infections and Antimicrobial Use Prevalence Survey Team. Multistate point prevalence survey of health care-associated infections. N Engl J Med 2014; 370:1198-208.
- Zilberberg MD, Shorr AF, Micek ST, Vazquez-Guillamet C, Kollef MH. Multi-drug resistance, inappropriate initial antibiotic therapy and mortality in Gram-negative severe sepsis and septic shock: A retrospective cohort study. Crit Care 2014; 18:596.
- Micek ST, Welch EC, Khan J, et.al. Resistance to empiric antimicrobial treatment predicts outcome in severe sepsis associated with Gram-negative bacteremia. J Hosp Med 2011; 6:405-10.
- Claudio Viscoli. Bloodstream Infections: The peak of the iceberg. Virulence 2016; 7: 248–51.
- Garner JS, Jarvis WR, Emori TG, et.al. CDC definitions for nosocomial infections, 1988. Am J Infect Control 1988, 16:128–40.
- Friedman ND, Kaye KS, Stout JE, et.al. Health care–associated bloodstream infections in adults: a reason to change the accepted definition of community-acquired infections. Ann Intern Med 2002, 137(10):791–7.
- Timsit JF, Soubirou JF, et al. Treatment of bloodstream infections in ICUs. BMC Infectious Diseases 2014, 14:489.
- Vallés J, Alvarez-Lerma F, et.al. Health-care-Associated Bloodstream Infections at Admission to the ICU CHEST 2011;139:810-5.
- Tabah A, Koulenti D, Laupland K, et.al. Characteristics and determinants of outcome of hospital-acquired bloodstream infections in intensive care units: the EUROBACT International Cohort Study Intensive Care Med (2012) 38:1930–45.
- Mermel L, Allon M, et.al. Guidelines for the Diagnosis and Management of Intravascular Catheter-Related Infection: 2009 Update by the Infectious Diseases Society of America. Clin Inf Dis 2009;49:1-45.
- Bassetti M, Righi E, Carnelutti A. Bloodstream infections in the Intensive Care Unit. Virulence 2016; VOL. 7, NO. 3, 267–79.
- Marik P E, Flemmer M, Harrison W. The risk of catheter-related bloodstream infection with femoral venous catheters as compared to subclavian and internal jugular venous catheters: A systematic review of the literature and meta-analysis Crit Care Med 2012; 40: 2479–85.
- O’Grady NP, Alexander M,. Burns LA, et.al. Guidelines for the Prevention Intravascular Catheter Related Infections Clin Infect Dis. 2011; 52: e162–e193.
- Vincent JL, Rello J, et al. International Study of the Prevalence and Outcomes of Infection in Intensive Care Units JAMA. 2009;302:2323-9.
- Ammerlaan HSM, Harbarth S, et.al. Secular Trends in Nosocomial Bloodstream Infections: Antibiotic-Resistant Bacteria Increase the Total Burden of Infection Clinical Infectious Diseases 2013;56:798–805.
- Maki DG, Kluger DM, Crnich CJ. The risk of bloodstream infection in adults with different intravascular devices: a systematic review of 200 published prospective studies. Mayo Clin Proc.2006;81:1159-71.
- Timsit JF. Diagnosis and prevention of catheter-related infections. Curr Opin Crit Care 2007; 13:563–71.
- Corona A, Bertolini G, et.al. Antibiotic use and impact on outcome from bacteraemic critical illness: the BActeraemia Study in Intensive Care (BASIC). J Antimicrob Chemother 2010; 65: 1276–85.
- Lim SJ, Choi JY, et.al. Intensive care unit-acquired blood stream infections: a 5-year retrospective analysis of a single tertiary care hospital in Korea. Infection 2014; 42:875–81.
- Warren DK, Zack JE, Elward AM, et al. Nosocomial primary bloodstream infections in intensive care unit patients in a nonteaching community medical center: a 21-month prospective study. Clin Infect Dis 2001; 33:1329–35.
- Timsit JF. Updating of the 12th consensus conference of the Societe de Reanimation de langue francaise (SRLF): catheter related infections in the intensive care unit. Ann Fr Anesth Reanim 2005;24:315–22.
- Lenz R, Leal JR, et al. The distinct category of healthcare associated bloodstream infections. BMC Infectious Diseases 2012, 12:85
- Kevin B. Laupland, Deirdre L. Church. Population-Based Epidemiology and Microbiology of Community-Onset Bloodstream Infections Clinical Microbiology Reviews 2014; 27:. 647–64.
- Wisplinghoff H, Bischoff T, et.al. Nosocomial Bloodstream Infections in US Hospital Analysis of 24,179 Cases from a Prospective Nationwide Surveillance Study Clinical Infectious Diseases 2004; 39:309–17
- Marra AR, Luis Fernando Aranha Camargo, et.al. Nosocomial Bloodstream Infections in Brazilian Hospitals: Analysis of 2,563 Cases from a Prospective Nationwide Surveillance Study J Clin Microbiol 2011, 49:1866–71.
- Dimopoulos G, Koulenti D, et.al. Bloodstream infections in ICU with increased resistance: epidemiology and outcomes. Minerva Anestesiol 2015;81:405-18.
- Timsit JF, ‘Heriteau FL, et.al. A multicentre analysis of catheter-related infection based on a hierarchical model. Intensive Care Med 2012; 38:1662–72.
- Fagan R, Jonathan R. Edwards, et.al, Incidence Trends in Pathogen-Specific Central Line–Associated Bloodstream Infections in US Intensive Care Units, 1990–2010 Infection Control and Hospital Epidemiology. September 2013;.34:893-99.
- Zilahi G, Artigas A, Ignacio Martin‑ What’s new in multidrug resistant pathogens in the ICU. Annals of Intensive Care 2016; 6:96.
- Karam G, Chastre J, Mark H, et al. Antibiotic strategies in the era of multidrug resistance. Critical Care 2016; 20:136.
- Lye DC, Earnest A, Ling ML, et.al. The impact of multidrug resistance in healthcare-associated and nosocomial Gram-negative bacteraemia on mortality and length of stay: cohort study. Clin Microbiol Infect 2012; 18: 502–8.
- Giamarellou et.al. Emergence of extensively drug-resistant and pandrug-resistant Gram-negative bacilli in Europe. Euro Surveill 2008,13:47.
- European Antimicrobial Resistance Surveillance Network (EARS-Net). EARSS Annual Report. 2013. Available at: http://ecdc.europa.eu/en/activities/surveillance/ EARS-Net. Last access 1 September 2017
- Kumar A, Ellis P, Arabi Y, et.al. Initiation of Inappropriate Antimicrobial Therapy Results in a Fivefold Reduction of Survival in Human Septic Shock. Chest 2009;136:1237-48.
- Retamar P, Portillo MM, López-Prieto MD, et.al. Impact of Inadequate Empirical Therapy on the Mortality of Patients with Bloodstream Infections: a Propensity Score-Based Analysis. Antimicrob Agents Chemother 2012, 56:472–8.
- Ferrer R, Martin-Loeches I, et al. Empiric Antibiotic Treatment Reduces Mortality in Severe Sepsis and Septic Shock From the First Hour: Results From a Guideline-Based Performance Improvement Program. Crit Care Med 2014, 42:1749–55.
- Lambert ML, Suetens C, Savey A, et alClinical outcomes of health-careassociated infections and antimicrobial resistance in patients admitted tο European intensive-care units: a cohort study. Lancet Infect Dis 2011;11:30–8.
- Marlieke E, de Kraker A, Davey PG, et al. Mortality and Hospital Stay Associated with Resistant Staphylococcus aureus and Escherichia coli Bacteremia: Estimating the Burden of Antibiotic Resistance in Europe. PLoS Med 2011; 8: e1001104.
- Pogue JM, Kaye KS, et.al. Appropriate antimicrobial therapy in the era of multidrug resistant human pathogens. Clin Microbiol Infect 2015;21:302-12.
- Peirano G, Laupland KB, Gregson DB, et.al. Colonization of returning travelers with CTX-M-producing Escherichia coli. J Travel Med 2011,18:299–303.
- Stralin K, Soderquist B: Staphylococcus aureus in community-acquired pneumonia. Chest 2006, 130:623.
- Woodhead M, Blasi F, Ewig S, et al. Guidelines for the management of adult lower respiratory tract infections–full version. Clin Microbiol Infect 2011, 17(Suppl 6):E1–E59.
- Nathwani D, Morgan M, Masterton RG, et al. Guidelines for UK practice for the diagnosis and management of methicillin-resistant Staphylococcus aureus (MRSA) infections presenting in the community. J Antimicrob Chemother 2008, 61(5):976–94.
- Safdar N, Handelsman J, Maki DG. Does combination antimicrobial therapy reduce mortality in Gram-negative bacteraemia? A meta-analysis. Lancet Infect Dis 2004; 4: 519–27.
- Lador PM A, Grozinsky-Glasberg S, Leibovici L. Beta lactam antibiotic monotherapy versus beta lactam aminoglycoside antibiotic combination therapy for sepsis (Review) The Cochrane Library 2014, Issue 1
- Peña C, Suarez C, Ocampo-Sosa A, et.al. Effect of Adequate Single-Drug vs Combination Antimicrobial Therapy on Mortality in Pseudomonas aeruginosa Bloodstream Infections: A Post Hoc Analysis of a Prospective Cohort. Clinical Infectious Diseases 2013;57:208–16.
- Vardakas KZ, Tansarli GS, Bliziotis IA, et.al. Beta-lactam plus aminoglycoside or fluoroquinolone combination versus beta-lactam monotherapy for Pseudomonas aeruginosa infections: a meta-analysis. Int J Antimicrob Agents 2013;41:301-10.
- Martínez JA, Cobos-Trigueros N, Soriano A, et.al. Influence of Empiric Therapy with a β-Lactam Alone or Combined with an Aminoglycoside on Prognosis of Bacteremia Due to Gram-Negative Microorganisms. Antimicrob Agents Chemother, Sept. 2010, p. 3590–96.
- Micek ST,. Welch EC, Khan J, et.al. Empiric Combination Antibiotic Therapy Is Associated with Improved Outcome against Sepsis Due to Gram-Negative Bacteria: a Retrospective Analysis. Antimicrob Agents Chemother 2010, 54:1742–48.
- Kumar A, Safdar N, et.al. A survival benefit of combination antibiotic therapy for serious infections associated with sepsis and septic shock is contingent only on the risk of death: A meta-analytic/meta-regression study. Crit Care Med 2010, 38:1651–64.
- Rhodes A, Evans LE, Alhazzani W, et.al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intensive Care Med. 2017;43:304-77.
- Tumbarello M, Sanguinetti M, Montuori E, et.al. Predictors of Mortality in Patients with Bloodstream Infections Caused by Extended-Spectrum-β-Lactamase-Producing Enterobacteriaceae: Importance of Inadequate Initial Antimicrobial Treatment. Antimicrob Agents Chemother 2007; 51:1987-94.
- Gutierrez-Gutierrez B, Bonomo RA, Carmeli Y, et al. Ertapenem for the treatment of bloodstream infections due to ESBL-producing Enterobacteriaceae: a multinational pre-registered cohort study. J Antimicrob Chemother 2016;71:1672-80.
- Rodriguez-Bano J, Cisneros JM, Cobos-Trigueros N, et al. Diagnosis and antimicrobial treatment of invasive infections due to multidrug-resistant Enterobacteriaceae. Guidelines of the Spanish Society of Infectious Diseases and Clinical Microbiology. Enferm Infecc Microbiol Clin 2015;33:337e1-e21.
- Bassetti M, De Waele JJ, Eggimann P, et al. Preventive and therapeutic strategies in critically ill patients with highly resistant bacteria. Intens Care Med 2015; 41:776-95.
- Harris PNA, Tambyah PA, Paterson DL. β-lactam and β-lactamase inhibitor combinations in the treatment of extended-spectrum β-lactamase producing Enterobacteriaceae: time for a reappraisal in the era of few antibiotic options? Lancet Infect Dis 2015.
- Gutierrez-Gutierrez B, Perez-Galera S, Salamanca E, et al. A multinational, preregistered cohort study of beta-lactam/ beta-lactamase inhibitor combinations for treatment of bloodstream infections due to extended-spectrum-beta lactamase-producing Enterobacteriaceae. Antimicrob Agents Chemother 2016;60:4159-69.
- Roberts JA, Paul SK, Akova M, et al. DALI: defining antibiotic levels in intensive care unit patients: are current beta-lactam antibiotic doses sufficient for critically ill patients? Clin Infect Dis 2014;58:1072-83.
- Kontopidou F, Giamarellou H, Katerelos P, et.al. Infections caused by carbapenem-resistant Klebsiella pneumoniae among patients in intensive care units in Greece: a multi-centre study on clinical outcome and therapeutic options. Clin Microbiol Infect 2014; 20: O117–O123.
- Tumbarello M, Viale P, Viscoli C, et.al. Predictors of Mortality in Bloodstream Infections Caused by Klebsiella pneumonia Carbapenemase–Producing K. pneumoniae: Importance of Combination Therapy. Clinical Infectious Diseases 2012;55:943–50.
- Tumbarello M, Trecarichi EM, De Rosa FG, et.al . Infections caused by KPC-producing Klebsiella pneumoniae: differences in therapy and mortality in a multicentre study. J Antimicrob Chemother 2015; 70: 2133–43.
- Qureshi ZA, Paterson DL, Potoski BA, et.al. Treatment Outcome of Bacteremia Due to KPC-Producing Klebsiella pneumoniae: Superiority of Combination Antimicrobial Regimens. Antimicrob Agents Chemother 2012; 56:2108-13.
- Daikos GL, Tsaousi S, Tzouvelekis LS, et al. Carbapenemase- producing Klebsiella pneumoniae bloodstream infections: lowering mortality by antibiotic combination schemes and the role of carbapenems. J Antimicrob Chemother 2014;58:2322-8.
- Zarkotou O, Pournaras S, Tselioti P, et.al. Predictors of mortality in patients with bloodstream infections caused by KPC-producing Klebsiella pneumoniae and impact of appropriate antimicrobial treatment. Clin Microbiol Infect 2011; 17: 1798–1803.
- Doi Y, Paterson DL. Carbapenemase-producing Enterobacteriaceae. Semin Respir Crit Care Med 2015;36:74-84.
- Perez F, El Chakhtoura NG, Papp-Wallace K, et al Treatment options for infections caused by carbapenem resistant Enterobacteriaceae: can we apply “precision medicine” to antimicrobial chemotherapy? Expert Opin Pharmacother. 2016;17:761-81.
- Rizek C, Ferraz JR, van der Heijden IM, et al. In vitro activity of potential old and new drugs against multidrugresistant gram-negatives. J Infect Chemother 2015;21:114-7.
- Poulakou G, Bassetti M, Righi E, Dimopoulos G. Current and future treatment options for infections caused by multidrug-resistant Gram-negative pathogens. Future Microbiol 2014;9:1053-69.
- Young-Mi Ah, Ah-Jung Kim, Ju-Yeun Lee. Colistin resistance in Klebsiella pneumonia. Int J Antimicrob Agents 2014; 44:8-15.
- Oliva A, Gizzi F, Mascellino MT, et al. Bactericidal and synergistic activity of double-carbapenem regimen for infections caused by carbapenemase-producing Klebsiella pneumoniae. Clin Microbiol Infect 2016 ; 22: 147–153.
- Poirel L, Kieffer N, Nordmann P. In vitro evaluation of dual carbapenem combinations against carbapenemaseproducing Enterobacteriaceae. J Antimicrob Chemother 2016;71:156-61.
- Cprek JB, Gallagher JC. Ertapenem-containing double carbapenem therapy for treatment of infections caused by carbapenem-resistant Klebsiella pneumoniae. Antimicrob Agents Chemother 2015;60:669-73.
- . Bassetti M, Pecori D, Peghin M. Multidrug-resistant Gram-negative bacteria-resistant infections: epidemiology, clinical issues and therapeutic options Italian Journal of Medicine 2016; 10:364-375.
- Batirel A, Balkan II, Karabay O, et al. Comparison of colistin-carbapenem, colistin-sulbactam, and colistin plus other antibacterial agents for the treatment of extremely drug-resistant Acinetobacter baumannii bloodstream infections. Eur J Clin Microbiol Infect Dis 2014;33:1311-22.
- Durante-Mangoni E, Signoriello G, Andini R, et al. Colistin and rifampicin compared with colistin alone for the treatment of serious infections due to extensively drug resistant Acinetobacter baumannii: a multicenter, randomized clinical trial. Clin Infect Dis 2013;57:349-58.
- Petrosillo N, Giannella M, Antonelli M, et al. Clinical experience of colistin-glycopeptide combination in critically ill patients infected with Gram-negative bacteria. Antimicrob Agents Chemother 2014;58:851-8.
- Sirijatuphat R, Thamlikitkul V. Preliminary study of colistin versus colistin plus fosfomycin for treatment of carbapenem- resistant Acinetobacter baumannii infections. Antimicrob Agents Chemother 2014;58:5598-601.
- Tumbarello M, Repetto E, Trecarichi EM, et al. Multidrug- resistant Pseudomonas aeruginosa bloodstream infections: risk factors and mortality. Epidemiol Infect 2011;139:1740-9.
- Parisi SG, Bartolini A, Santacatterina E, et al. Prevalence of Klebsiella pneumoniae strains producing carbapenemases and increase of resistance to colistin in an Italian teaching hospital from January 2012 To December 2014. BMC Infectious Diseases (2015) 15:244.
- Humphries RM, Kelesidis T, Dien Bard J, et al. Successful treatment of pan-resistant Klebsiella pneumoniae pneumoniaand bacteraemia with a combination of high-dose tigecycline and colistin. J Med Microbiol 2010;59:1383–6.
- Zusman O, Avni T, Leibovici L, et al. Systematic review and meta-analysis of in vitro synergy of polymyxins and carbapenems. Antimicrob Agents Chemother 2013;57: 5104–11.
- Pontikis K, Karaiskos I, Bastani S, et al. Outcomes of critically ill intensive care unit patients treated with fosfomycin for infections due to pandrug-resistant and extensively drug-resistant carbapenemase-producing Gram-negative bacteria. Int J Antimicrob Agents2014;43:52–9.
- Souli M, Galani I, Boukovalas S, et al. In vitro interactions of antimicrobial combinations with fosfomycin against KPC-2-producing Klebsiella pneumoniae and protection of resistance development. Antimicrob Agents Chemother 2011;55:2395–7.
- Liu C, Bayer A, et.al. Clinical Practice Guidelines by the Infectious Diseases Society of America for the Treatment of Methicillin- Resistant Staphylococcus aureus Infections in Adults and Children. Clinical Infectious Diseases 2011;52(3):e18–e55.
- Moore CL, Osaki-Kiyan P, Haque NZ, et al. Daptomycin versus vancomycin for bloodstream infections due to methicillin-resistant Staphylococcus aureus with a high vancomycin minimum inhibitory concentration: a case-control study. Clin Infect Dis 2012; 54:51-8.
- Murray KP, Zhao JJ, Davis SL, et al. Early use of daptomycin versus vancomycin for methicillin-resistant Staphylococcus aureus bacteremia with vancomycin minimum inhibitory concentration >1 mg/L: a matched cohort study. Clin Infect Dis 2013; 56:1562-9.
- Bauer J, Siala W, Tulkens PM, et al. A combined pharmacodynamic quantitative and qualitative model reveals the potent activity of daptomycin and delafloxacin against Staphylococcus aureus biofilms. Antimicrob Agents Chemother 2013; 57:2726-37.
- Bassetti M, Ansaldi F, De Florentiis D, et al. Is empiric daptomycin effective in reducing mortality in Staphylococcus aureus bacteraemia? A real-life experience. Intensive Care Med 2015; 41:2026-8.
- Poulikakos P, Tansarli GS, Falagas ME. Combination antibiotic treatment versus monotherapy for multidrug resistant, extensively drug-resistant, and pandrug-resistant Acinetobacter infections: a systematic review. Eur J Clin Microbiol Infect Dis 2014;33:1675-85.
- Mokart D, Slehofer G, Lambert J, et al. De-escalation of antimicrobial treatment in neutropenic patients with severe sepsis: Results from an observational study. Intensive Care Med 2014; 40:41-9.
- Garnacho-Montero J, A. Gutierrez-Pizarraya A. Escoresca-Ortega et.al. De-escalation of empirical therapy is associated with lower mortality in patients with severe sepsis and septic shock Intensive Care Med 2014; 40:32-40.
- Marc L, Bechis C, Baumstarck K, et.al. De-escalation versus continuation of empirical antimicrobial treatment in severe sepsis: a multicenter non-blinded randomized noninferiority trialIntensive Care Med 2014;40:1399-408.
- Havey TC, Fowler RA, Daneman N. Duration of antibiotic therapy for bacteremia: A systematic review and meta-analysis. Crit Care 2011; 15:R267.
- Danemana, K. Shorea, et.al. Antibiotic treatment duration for bloodstream infections in critically ill patients: a national survey of Canadian infectious diseases and critical care specialists International Journal of Antimicrobial Agents 2011; 38:480– 5.
- Rubinstein, Y. Keynan. Short-course therapy for severe infections Int J Antimicrob Agents 2013; 42 Suppl:S22-4.
- Prkno et al. Procalcitonin-guided therapy in intensive care unit patients with severe sepsis and septic shock – a systematic review and meta-analysis Critical Care 2013, 17:R291.
- Matthaiou D, Ntani G, et.al An ESICM systematic review and meta-analysis of procalcitonin-guided antibiotic therapy algorithms in adult critically ill patients Intensive Care Med 2012; 38:940–9.
- Boyer A, Vargas F, Coste F, et al: Influence of surgical treatment timing on mortality from necrotizing soft tissue infections requiring intensive care management. Intensive Care Med 2009, 35:847–53.
- Infectious Diseases Society of America/American Thoracic Society Consensus Guidelines on the Management of Community-Acquired Pneumonia in Adults, Clinical Infectious Diseases 2007; 44:S27–72.
- Kalil AC, Metersky ML, Klompas M, et.al. Management of Adults With Hospital-acquired and Ventilator-associated Pneumonia: 2016 Clinical Practice Guidelines by the Infectious Diseases Society of America and the American Thoracic Society
- Solomkin JS, Mazuski JE, Bradley JS, et al: Diagnosis and management of complicated intra-abdominal infection in adults and children: guidelines by the Surgical Infection Society and the Infectious Diseases Society of America. Clin Infect Dis 2010, 50:133–64.
- Stevens DL, Bisno AL, et al: Practice guidelines for the diagnosis and management of skin and soft tissue infections: 2014 update by the Infectious Diseases Society of America. Clin Infect Dis 2014, 59:e10–e52.
- Hooton TM, Bradley SF, et al: Diagnosis, prevention, and treatment of catheter-associated urinary tract infection in adults: 2009 International Clinical Practice Guidelines from the Infectious Diseases Society of America. Clin Infect Dis 2010, 50(5):625–663
- Akova M. Epidemiology of antimicrobial resistance in bloodstream infections. Virulence 2016;7: 252–66.
Author Disclosures:
Authors Schizodimos Th., Soulountsi V. have no conflicts of interest or financial ties to disclose.
Corresponding author:
Soulountsi Vasiliki, MD,
Papanikolaou Hospital, Exohi 570 10,
Thessaloniki, Greece
e-mail:









