Authors: Πεζήκογλου Ι. MD1, Φυντανίδου Β. MD, PhD2, Φορούλης Χ. MD, PhD3, Αμανίτη Α. MD, PhD1, Αλεξίου Ι. MD, MSc3, Κυπαρισσά Μ. MD, PhD1, Παλάσκα Ε. MD1, Γροσομανίδης Β. MD, PhD1.
1Κλινική Αναισθησιολογίας και Εντατικής Θεραπείας Α.Π.Θ, Π.Γ.Ν.Θ ΑΧΕΠΑ, Θεσσαλονίκη
2Τμήμα Επειγόντων Περιστατικών Π.Γ.Ν.Θ ΑΧΕΠΑ, Θεσσαλονίκη
3Καρδιοθωρακοχειρουργική κλινική Α.Π.Θ, Π.Γ.Ν.Θ ΑΧΕΠΑ, Θεσσαλονίκη
Abstract
Pneumothorax is a collection of air in the pleural space between the lungs and the chest wall and depending on its cause it could be either spontaneous or traumatic. Tension Pneumothorax (TPT) can be a cause of cardiac arrest (CA) or might be a complication after chest compressions. According to the 2015 European Resuscitation Council guidelines on resuscitation, TP is considered one of the reversible causes of CA, which should be recognized and treated during cardiopulmonary resuscitation (CPR). A 61yrs old patient (ASA-PS:3, NYHA:2) was scheduled for a video-assisted mesothoracoscopy. The patient was a former smoker and suffered from hypertension and chronic obstructive pulmonary disease. He underwent an uneventful video-assisted mesothoracoscopy, was extubated in the operating theatre and was transferred to the High Dependency Unit. Approximately 40min later and after a prolonged cough episode, he experienced severe dyspnea, tachypnea, tachycardia, hypertension, SpO2 reduction and he became anxious. A bedside chest x-ray has been already performed before this episode but the image was not yet available to the physicians. Patient deteriorated very fast, he became agitated, experienced a severe blood pressure decrease, which was followed by CA. The initial CA rhythm was Pulseless Electrical Activity (PEA). CPR was initiated immediately with chest compressions, mask ventilation and intravenous administration of 1mg adrenaline. After endotracheal intubation it was impossible to ventilate the (intubated) patient with a bag-valve device. Esophageal Intubation was excluded since endotracheal intubation has been performed by an experienced consulting anesthesiologist and the direct laryngoscopy was easy and classified as Cormack-Lehane grade 1 and therefore tension pneumothorax was highly suspected. Immediately at this time point two chest tubes were inserted bilaterally without any interruption of the chest compressions. Air was expelled only from the right chest. CA rhythm remained PEA and Return of Spontaneous Circulation (ROSC) was achieved after 5min of CPR and without administration of a second adrenaline dose. After ROSC, patient was transferred to the Intensive Care Unit, where he was extubated the next day without any neurological deficits and thereafter he experienced an uneventful recovery. Pneumothorax is one of the possible complications of video-assisted mesothoracoscopy, while TPT is a reversible cause of CA. Recognition of CA, immediate CPR initiation and early diagnosis and treatment of TPT contributed to short CA-ROSC time and to the survival of this patient without any neurological impairment.
ΕΙΣΑΓΩΓΗ
Πνευμοθώρακας είναι η συλλογή αέρα στην υπεζωκοτική κοιλότητα και ανάλογα με την αιτία του μπορεί να είναι αυτόματος ή τραυματικός. Ειδική κατηγορία τραυματικού πνευμοθώρακα αποτελεί ο ιατρογενής, καθώς προκαλείται από ιατρικές παρεμβάσεις (τοποθέτηση κεντρικών φλεβικών γραμμών, παρακέντηση πλευριτικών συλλογών)1.
Η συλλογή αέρα στην υπεζωκοτική κοιλότητα αρχικά συμπιέζει τον πνεύμονα και προκαλεί υποξία ενώ καθώς η πίεση συνεχίζει να αυξάνεται μετακινεί το μεσοθωράκιο προς την υγιή πλευρά, η φλεβική επιστροφή μειώνεται και οδηγεί τον ασθενή σε αιμοδυναμική κατάρρευση1.
Ο απλός πνευμοθώρακας είναι διαφορετική νοσολογική οντότητα από τον πνευμοθώρακα υπό τάση, ο οποίος είναι κατάσταση απειλητική για τη ζωή, και αποτελεί αιτία καρδιακής ανακοπής2.
Με βάση τις συστάσεις των επιστημονικών εταιρειών, σε κάθε περίπτωση υποψίας πνευμοθώρακα υπό τάση θα πρέπει να γίνεται άμεσα αποσυμπίεση του, χωρίς αναμονή για χρονοβόρες διαγνωστικές εξετάσεις2,3.
Ο πνευμοθώρακας μπορεί να προκαλέσει καρδιακή ανακοπή αλλά και μπορεί να προκληθεί από την εφαρμογή των θωρακικών συμπιέσεων κατά τη διάρκεια Καρδιοπνευμονικής Αναζωογόνησης (ΚΑΡΠΑ)2,4,5.
Σύμφωνα με τις κατευθυντήριες οδηγίες για την αναζωογόνηση 2015, του Ευρωπαϊκού Συμβουλίου Αναζωογόνησης (ERC) ο πνευμοθώρακας συμπεριλαμβάνεται στα αναστρέψιμα αίτια καρδιακής ανακοπής και θα πρέπει να αναγνωρίζεται και να αντιμετωπίζεται κατά την διάρκεια ΚΑΡΠΑ6. Παρά το ότι η διάγνωση είναι κλινική, δεν είναι πάντα εύκολη και χρειάζεται υψηλός δείκτης υποψίας για την πρόληψη αλλά και την αντιμετώπιση της καρδιακής ανακοπής που οφείλεται σε πνευμοθώρακα2,6. Η μη αναγνώριση του και η άμεση αντιμετώπιση του μηδενίζει την πιθανότητα επανόδου της αυτόματης κυκλοφορίας (ROSC)7.
Η μεσοθωρακοσκόπηση περιγράφηκε το 1959 από τον Carlens, αποτελεί μία ελάχιστα επεμβατική χειρουργική επέμβαση που πραγματοποιείται για τη σταδιοποίηση νεοπλασμάτων του πνεύμονα αλλά και για διαγνωστικούς σκοπούς (λεμφώματα)8.Έχει υψηλού βαθμού (>80%) ευαισθησία και ειδικότητα(100%) για την σταδιοποίηση του καρκίνου του πνεύμονα9.
Με την ανάπτυξη νέων απεικονιστικών εξετάσεων (ποζιτρονική τομογραφία – PETscan) υπάρχει μια τάση μείωσης των μεσοθωρακοσκοπήσεων χωρίς όμως να έχει χάσει την αξία της10.
Οι επιπλοκές της επέμβασης δεν είναι συχνές αλλά μπορεί να είναι δυνητικά θανατηφόρες. Ο πνευμοθώρακας αποτελεί μια από τις αναφερόμενες επιπλοκές της μεσοθωρακοσκόπησης.
Στην παρούσα αναφορά περιστατικού παρουσιάζουμε έναν ασθενή ο οποίος υπέστη καρδιακή ανακοπή οφειλόμενη σε πνευμοθώρακα υπό τάση μετά από διατραχηλική μεσοθωρακοσκόπηση.
ΠΑΡΟΥΣΙΑΣΗ ΠΕΡΙΣΤΑΤΙΚΟΥ
Ασθενής άνδρας ηλικίας 61 ετών, με νεόπλασμα αριστερού πνεύμονα (εικ. 1), ταυτοποιηθέν ως αδενοκαρκίνωμα βάσει της κυτταρολογικής έκθεσης μετά από βρογχοσκόπηση, προσήλθε προγραμματισμένα για διενέργεια διατραχηλικής μεσοθωρακοσκόπησης με στόχο τη λήψη λεμφαδένων για βιοψία και σταδιοποίηση της νόσου. Από το ατομικό αναμνηστικό, αναφέρεται ότι ο ασθενής ήταν πρώην καπνιστής (διακοπή προ 10ετίας) με εμφυσηματικού τύπου Χρόνια Αποφρακτική Πνευμονοπάθεια (ΧΑΠ). Κατά την προεγχειρητική σπιρομέτρηση, οι τιμές FVC και FEV1 ήταν στο 56 και 57 % των προβλεπόμενων τιμών, αντίστοιχα. Επίσης στο ατομικό του ιστορικό αναφέρεται και η αρτηριακή υπέρταση, ενώ η φαρμακευτική του αγωγή περιελάμβανε εισπνεόμενα και αντιυπερτασικά φάρμακα. Στην προεγχειρητική αναισθησιολογική εκτίμηση ο ασθενής κατατάχθηκε στην κατηγορία ΙΙΙ κατά ASA – PS και στην κατηγορία ΙΙ κατά NYHA.
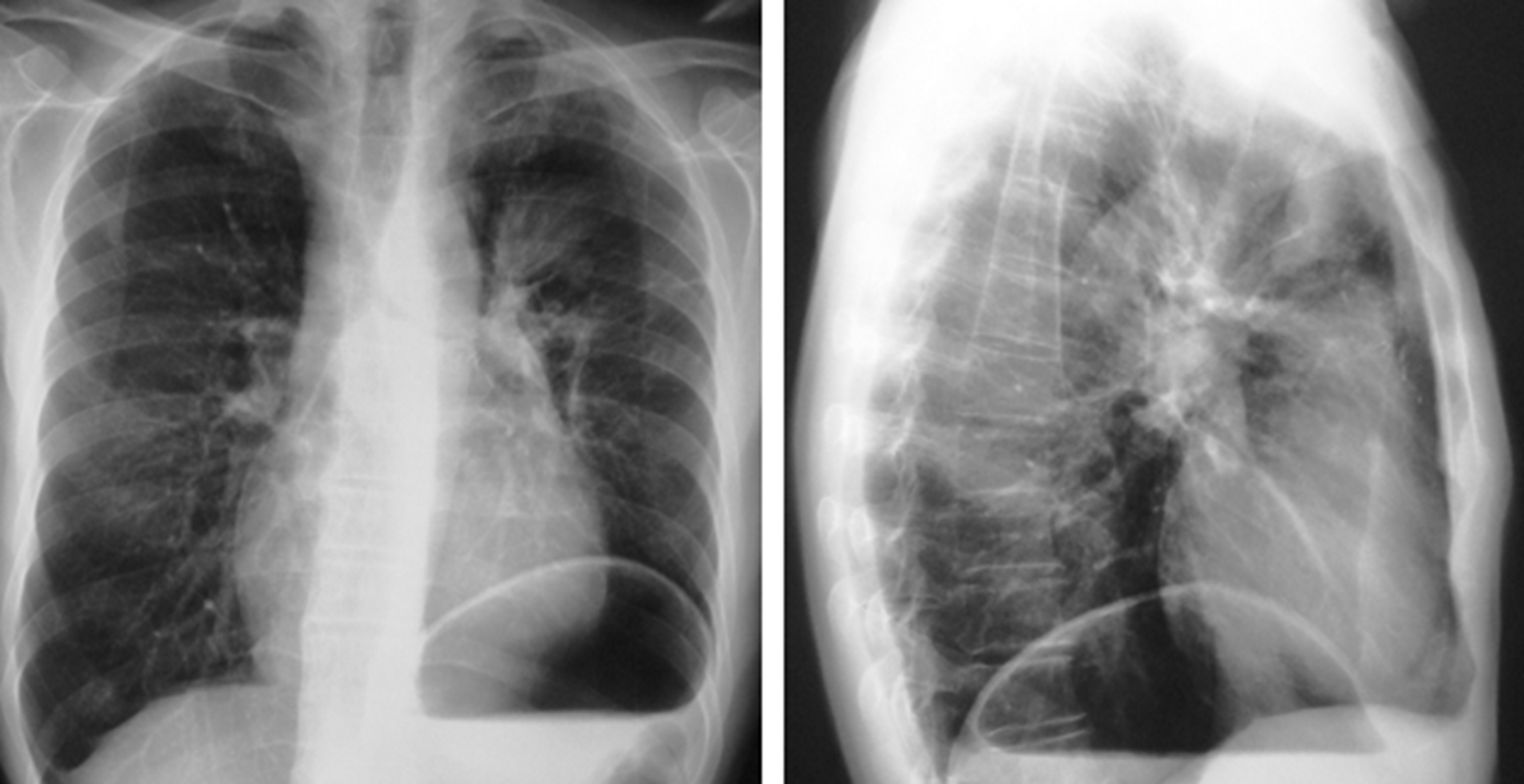
Εικόνα 1. Προεγχειρητική ακτινογραφία θώρακα.
Η εισαγωγή στην αναισθησία ήταν ομαλή, ενώ επιλέχθηκε προστατευτικός μηχανικός αερισμός με εισπνεόμενο όγκο 7ml/kgΣΒ και 12 αναπνοές ανά λεπτό. Εκτός του βασικού monitoring, για την συνεχή παρακολούθηση της συστηματικής αρτηριακής πίεσης και για την αναγνώριση πιθανών χειρισμών επί της ανωνύμου αρτηρίας, καθετηριάστηκε η δεξιά κερκιδική αρτηρία.
Η χειρουργική επέμβαση ήταν σύντομης διάρκειας και ανεπίπλεκτη και ο ασθενής παρέμεινε αιμοδυναμικά και αεριομετρικά σταθερός καθ’ όλη τη διάρκεια της. Μετά το τέλος της επέμβασης ο ασθενής αποδιασωληνώθηκε και μεταφέρθηκε στη μονάδα αυξημένης φροντίδας της καρδιοχειρουργικής κλινικής. Πριν από την αποδιασωλήνωση και πριν από την αναχώρηση από την χειρουργική αίθουσα έγινε ακρόαση των πνευμόνων (ομότιμο αναπνευστικό ψιθύρισμα), ενώ πριν την αποσύνδεση του ασθενούς από το monitor οι τιμές των ζωτικών σημείων ήταν καρδιακή συχνότητα (ΚΣ):70b/min, αριθμός αναπνοών (ΑΑ):14/min, αρτηριακή πίεση (ΑΠ):140/75mmHg, ενώ ο κορεσμός της αιμοσφαιρίνης σε οξυγόνο(SpO2):99% με απλή μάσκα οξυγόνου στα 8l/min.
Στον ασθενή, κατά τη μεταφορά, εχορηγείτο οξυγόνο με μάσκα στα 8l/min, ενώ με τη σύνδεση στο monitor μετά την άφιξη στη μονάδα αυξημένης φροντίδας, είχε ΚΣ:75b/min, SpO2:98% (με απλή μάσκα οξυγόνου), AΑ: 15/min, και ΑΠ:150/80mmHg.
Σαράντα λεπτά αργότερα, μετά από παρατεταμένο βήχα, ο ασθενής εκδήλωσε έντονη δύσπνοια, ταχύπνοια, ταχυκαρδία, πτώση του SpO2 και υπέρταση, ενώ άρχισε να γίνεται ανήσυχος. Είχε προηγηθεί ακτινογραφία θώρακα επί κλίνης, στα πλαίσια πρωτοκόλλου ρουτίνας εισαγωγής ασθενούς στη μονάδα αυξημένης φροντίδας, χωρίς να είναι ακόμα γνωστά τα ευρήματα της.
Λόγω της αιφνίδιας επιδείνωσης, έγινε κλήση βοήθειας από τους εφημερεύοντες ιατρούς της κλινικής. Κατά την αρχική εκτίμηση κατά ABCDE, ο ασθενής είχε ελεύθερο αεραγωγό, ταχύπνοια (μικρές επιπόλαιες αναπνοές με ασυνέργεια κοιλιακών και θωρακικών μυών (ΑΑ:35/min), SpO2:75% με απλή μάσκα και ρινική χορήγηση οξυγόνου, ταχυκαρδία (ΚΣ:120b/min), υπέρταση (ΑΠ:170/90 mmHg). Επίσης ο ασθενής ήταν διεγερτικός με διατεταμένες σφαγίτιδες και εικόνα συμφόρησης από τις κλείδες και πάνω. Ακροαστικά υπήρχε μείωση του αναπνευστικού ψιθυρίσματος, αλλά λόγω των συνθηκών και του τρόπου αναπνοής δεν καταγράφηκε διαφορά μεταξύ των δύο ημιθωρακίων.
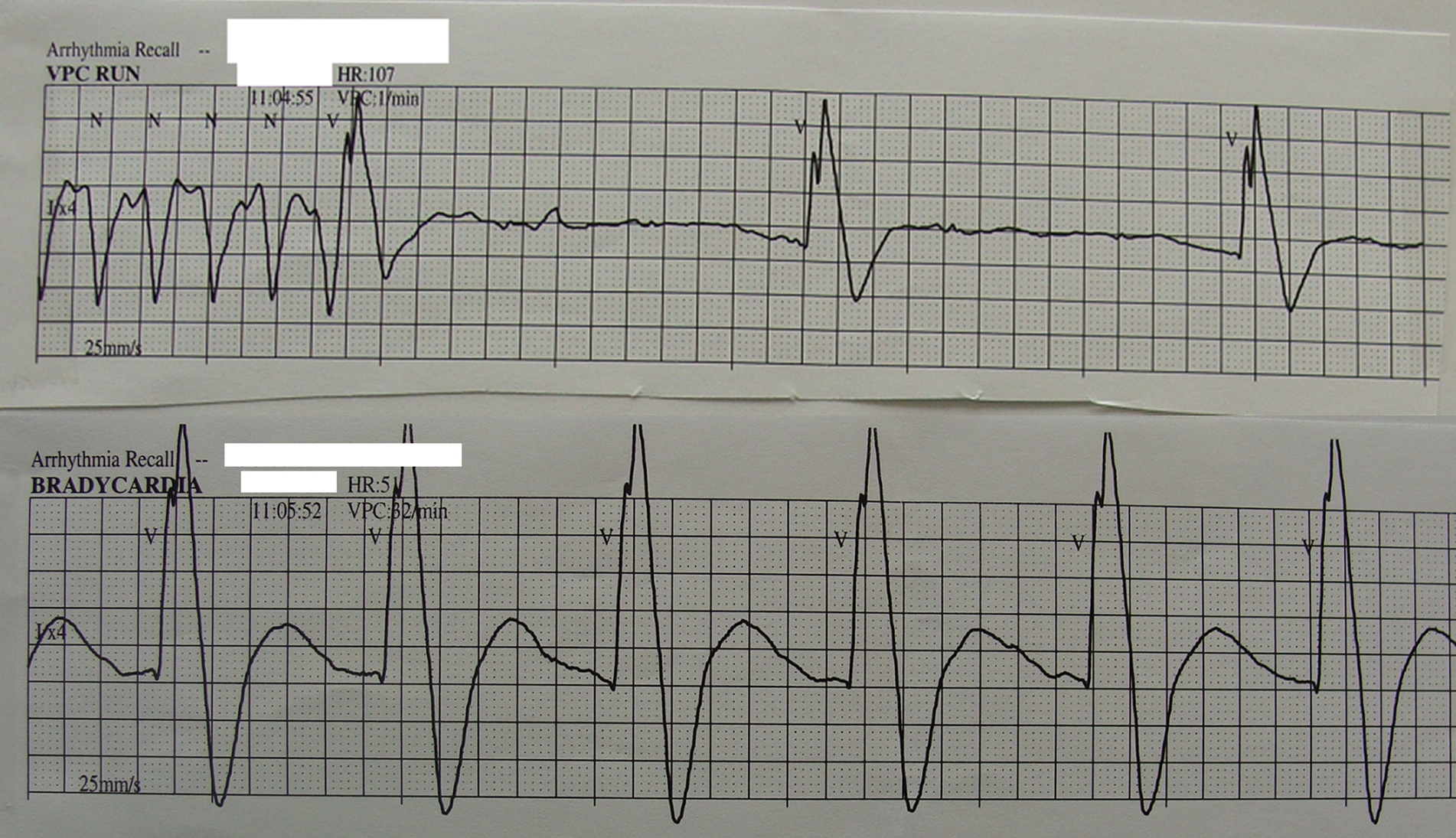
Άμεσα έγινε σκέψη για κλιμάκωση φροντίδας και μεταφορά στη ΜΕΘ, αλλά προτού να γίνει οποιαδήποτε παρέμβαση, οασθενεής παρουσίασε πτώση της ΚΣ (εικ. 2), απώλεια συνείδησης, αδυναμία ψηλάφησης σφύξεων στην καρωτίδα και gasping.

Εικόνα 2. Αρχικός ρυθμός καρδιακής ανακοπής (Άσφυγμη Ηλεκτρική Δραστηριότητα).
Η κατάσταση αυτή αναγνωρίστηκε ως καρδιακή ανακοπή. Έγινε έναρξη καρδιοπνευμονικής αναζωογόνησης με θωρακικές συμπιέσεις αερισμό και χορήγηση 1mg αδρεναλίνης ενδοφλεβίως (εικ. 3). Μετά τη στοματοτραχειακή διασωλήνωση διαπιστώθηκε αδυναμία αερισμού με αυτοδιατεινόμενο ασκό (Ambu). Καθώς η διασωλήνωση ήταν ευχερής (Cormack-Lehane grade Ι), η οποία έγινε από ειδικό αναισθησιολόγο, αποκλείστηκε από την αρχή η πιθανότητα διασωλήνωσης οισοφάγου και μπήκε η υποψία πνευμοθώρακα υπό τάση.

Εικόνα 3. Καρδιακός ρυθμός υπό Θωρακικές συμπιέσεις (ΚΑΡΠΑ).
Χωρίς τη διακοπή των θωρακικών συμπιέσεων έγινε άμεση τοποθέτηση σωλήνων θωρακικής παροχέτευσης αμφοτερόπλευρα. Αέρας υπό πίεση βγήκε μόνο από το αριστερό ημιθωράκιο. Ο ρυθμός παρέμεινε άσφυγμη ηλεκτρική δραστηριότητα (εικ. 4), χορηγήθηκε επαναληπτική δόση (1mg) αδρεναλίνης και επιτεύχθηκε ROSC μετά από 5 min συνολικής διάρκειας ΚΑΡΠΑ (εικ.5).
Εικόνα 4. Ο καρδιακός ρυθμός παραμένει Ασφυγμη Ηλεκτρική Δραστηριότητα
Εικόνα 4. Ο καρδιακός ρυθμός παραμένει Ασφυγμη Ηλεκτρική Δραστηριότητα
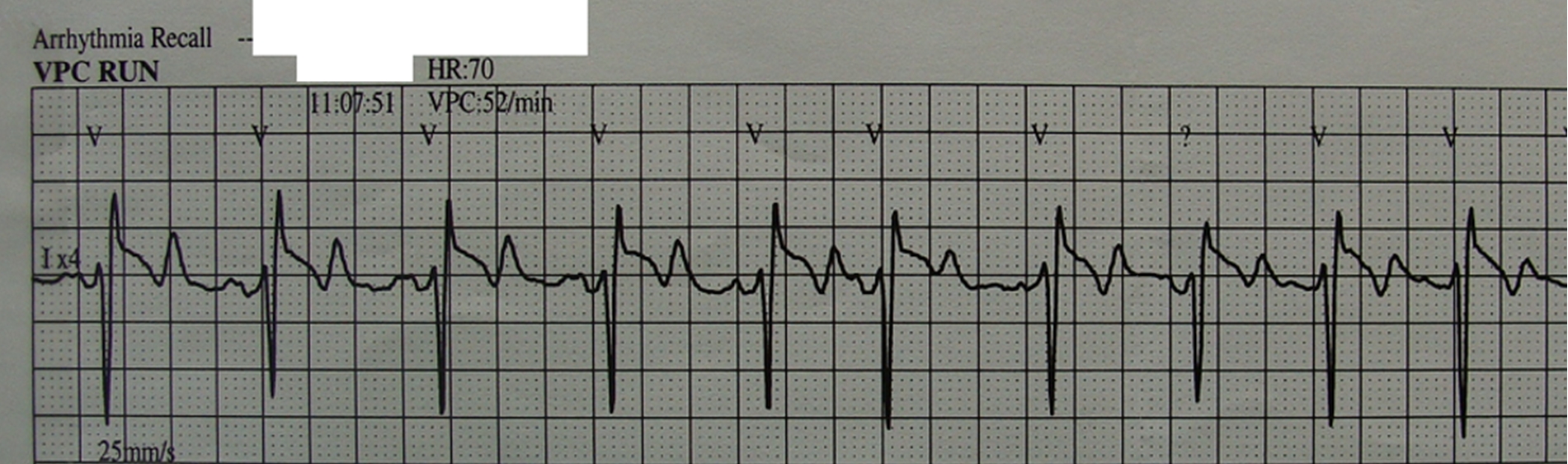
Εικόνα 5. Επάνοδος της αυτόματης κυκλοφορίας μετά από 5 min εφαρμογής ΚΑΡΠΑ
Ο ασθενής μετά την επίτευξη ROSC μεταφέρθηκε στην ΜΕΘ και αποδιασωληνώθηκε είκοσι ώρες αργότερα, χωρίς νευρολογικά ελλείματα.
Η εμφάνιση του φιλμ της ακτινογραφίας που είχε προηγηθεί της ανακοπής αποκάλυψε υπό πνευμοθώρακα δεξιά (εικ.6).
Εικόνα 6. Μετεγχειρητική ακτινογραφία θώρακα επί κλίνης, στην οποία διακρίνεται πνευμοθώρακας δεξιά. Η ακτινογραφία είχε γίνει προ κλινικής επιδείνωσης του ασθενούς
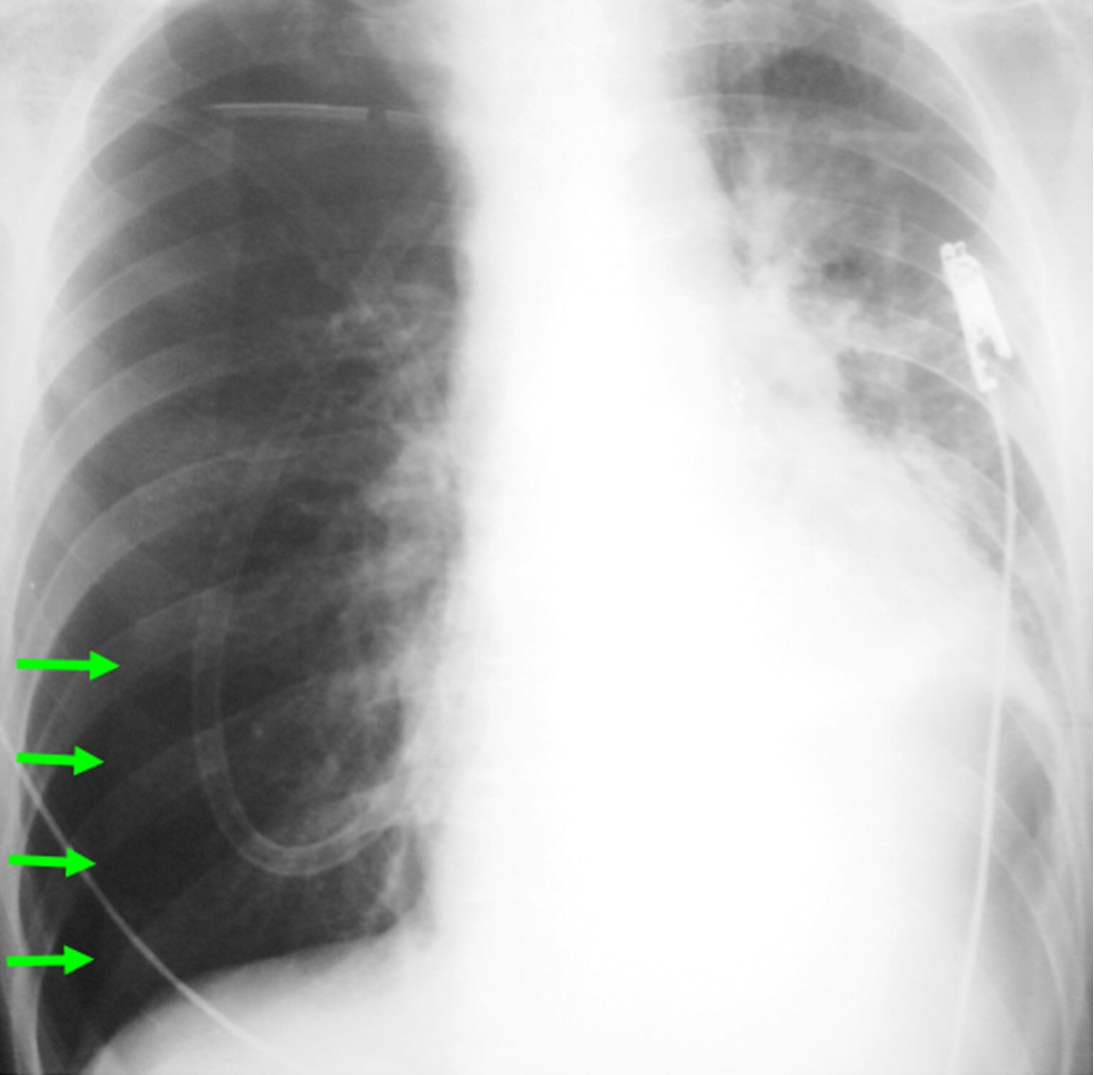
Εικόνα 6. Μετεγχειρητική ακτινογραφία θώρακα επί κλίνης, στην οποία διακρίνεται πνευμοθώρακας δεξιά. Η ακτινογραφία είχε γίνει προ κλινικής επιδείνωσης του ασθενούς
Η μετέπειτα πορεία του ήταν ομαλή χωρίς ιδιαίτερα προβλήματα και ο ασθενής εξήλθε από το νοσοκομείο σε καλή κατάσταση (εικ. 7).
Εικόνα 7. Ακτινογραφία εξόδου από το νοσοκομείο

Εικόνα 7. Ακτινογραφία εξόδου από το νοσοκομείο
ΣΥΖΗΤΗΣΗ
Ο ασθενής υποβλήθηκε σε προγραμματισμένη τραχηλική μεσοθωρακοσκόπηση για τη σταδιοποίηση αδενοκαρκινόματος (σύμφωνα με την προηγηθείσα κυτταρολογική εξέταση) του αριστερού πνεύμονα. Η μεσοθωρακοσκόπηση παρά την ανάπτυξη σύγχρονων απεικονιστικών εξετάσεων παραμένει ως εξέταση εκλογής για τη σταδιοποίηση νεοπλασμάτων του πνεύμονα αλλά και για διαγνωστικούς σκοπούς. Πραγματοποιείται υπό γενική αναισθησία, δεν απαιτεί τραχειοσωλήνα διπλού αυλού, ενώ υπάρχουν αναφορές και για χρήση λαρυγγικής μάσκας12. Διεγχειρητικά προβλήματα που μπορεί να εμφανισθούν είναι υπέρταση, ταχυκαρδία, αιμορραγία, προβλήματα από πίεση της ανώνυμης αρτηρίας13.
Η τοποθέτηση μίας ή δύο περιφερικών φλεβικών γραμμών αρκεί, αν και μερικοί συγγραφείς προτείνουν την τοποθέτηση μηριαίας φλέβας για την πιθανότητα αντιμετώπισης αιμορραγίας, η οποία όμως δεν είναι συχνή14,15. Η άμεση μέτρηση της αρτηριακής πίεσης προτιμάται από τους περισσότερους αναισθησιολόγους καθώς βοηθάει για την ταχεία αναγνώριση αντανακλαστικών αρρυθμιών και πίεσης στα μεγάλα αγγεία. Για την τοποθέτηση αρτηριακής γραμμής προτιμάται η δεξιά κερκιδική αρτηρία, για την αναγνώριση μεταβολών λόγω πίεσης, από χειρουργικούς χειρισμούς, στην ανώνυμη αρτηρία. Εναλλακτικά, μπορεί να χρησιμοποιηθεί η κυματομορφή από το παλμικό οξύμετρο το οποίο θα πρέπει να τοποθετεί στην δεξιά πλευρά.
Μετά το τέλος της επέμβασης ο ασθενής αφυπνίστηκε και μεταφέρθηκε στη μονάδα αυξημένης φροντίδας της κλινικής, πληρώντας τα κριτήρια εξόδου από τη χειρουργική αίθουσα16,17.
Η αμεσοσκόπηση είναι μια αξιόπιστη και ασφαλής επέμβαση, αποτελεί μια επέμβαση ρουτίνας όταν εκτελείται από εκπαιδευμένους θωρακοχειρουργούς, αλλά όπως όλες οι χειρουργικές επεμβάσεις δεν είναι άμοιρη επιπλοκών18. Οι επιπλοκές της επέμβασης αν και σπάνιες μπορεί να είναι επικίνδυνες για τη ζωή με τη νοσηρότητα να κυμαίνεται μεταξύ 0,6% και 2,3% και τη θνητότητα από 0-0,05%. Οι συχνότερα αναφερόμενες επιπλοκές είναι αιμορραγία, πνευμοθώρακας, εμμένουσα βλάβη στο λαρυγγικό νεύρο που προκαλεί βράγχος φωνής, λοιμώξεις, κάκωση στο φρενικό νεύρο, κάκωση στον οισοφάγο, χυλοθώρακας, αεριώδης εμβολή11,19,20. Οι πιο επικίνδυνες επιπλοκές είναι η μαζική αιμορραγία λόγω τρώσης της ανωνύμου αρτηρίας ή κάποιου άλλου μεγάλου αγγείου, καθώς και ο πνευμοθώρακας που συνήθως εντοπίζεται δεξιά19,21.Η αιμορραγία στην πλειονότητα των περιπτώσεων ελέγχεται με επιπωματισμό, ενώ σε ένα μικρό ποσοστό (0,4% ) θα χρειασθεί στερνοτομή ή θωρακοτομή21.
Ο Puhakka, σε μια σειρά 2021 μεσαυλιοσκοπήσεων, ανέφερε ποσοστό επιπλοκών 2,3 %, το συνολικό ποσοστό σοβαρών επιπλοκών ήταν 0,5%, ενώ καμία από αυτές δεν ήταν θανατηφόρος22. Οι Hammoud και συν. σε 2137 ασθενείς που υποβλήθηκαν σε μεσοθωρακοσκόπηση αναφέρουν 12 επιπλοκές και 4 περιεγχειρητικούς θανάτους. Από τους αναφερόμενους θανάτους μόνο ένας αποδόθηκε άμεσα στην επέμβαση και αφορούσε ρήξη αορτής. Σε έναν από τους 12 ασθενείς, η επιπλοκή ήταν πνευμοθώρακας23.
Οι Lemaire και συν. σε μια αναδρομική μελέτη (από ένα μόνο κέντρο) σε 2145 αμεσοσκοπήσεις ανέφεραν επιπλοκές σε 23 (1,07%) ασθενείς. Από τους 23 αυτούς ασθενείς οι 7 (0,33%) είχαν αιμορραγία, οι 12 (0,55%) βράγχος φωνής από βλάβη στο λαρυγγικό νεύρο, οι 2 (0,09%) κάκωση στην τραχεία και οι 2 (0,09%) πνευμοθώρακα. Από αυτούς απεβίωσε 1 (0,05%) από αιμορραγία λόγω κάκωσης της πνευμονικής αρτηρίας24.
Η συλλογή αέρα στην υπεζωκοτική κοιλότητα οδηγεί στην απώλεια της αρνητικής πίεσης μεταξύ των δύο πετάλων του υπεζωκότα και συμπίεση του πνεύμονα. Ανεξαρτήτου αιτίας ο απλός πνευμοθώρακας μπορεί να εξελιχθεί σε πνευμοθώρακα υπό τάση, ο οποίος οδηγεί σε θάνατο εάν δεν αναγνωρισθεί και αντιμετωπισθεί άμεσα.Η συχνότητα και η ταχύτητα εξέλιξης ενός απλού πνευμοθώρακα σε υπό τάση καθώς και οι παράγοντες που σχετίζονται με αυτό δεν είναι καταγεγραμμένα25.
Ωστόσο, φαίνεται ότι η μηχανική υποστήριξη της αναπνοής με θετικές πιέσεις αποτελεί παράγοντα κινδύνου, τόσο για την πρόκληση πνευμοθώρακα όσο και την συχνότερη και ταχύτερη εξέλιξη του απλού σε πνευμοθώρακα υπό τάση26,27.
Ο πνευμοθώρακας ως κλινική οντότητα συναντάται περισσότερο συχνά προνοσοκομειακά στους τραυματίες, στο τμήμα επειγόντων περιστατικών και στη ΜΕΘ1,27. Διεγχειρητικά μπορεί να εμφανισθεί από χειρουργικούς χειρισμούς, τοποθέτηση κεντρικών φλεβικών γραμμών, διενέργεια περιφερικών νευρικών αποκλεισμών και μηχανικό αερισμό28,29. Για τους ασθενείς της ΜΕΘ αποτελεί μια δυνητικά θανατηφόρο επιπλοκή του μηχανικού αερισμού και είναι ανεξάρτητη παράμετρος θνητότητας30. Παρά το ότι είναι δυνητικά θανατηφόρος κατάσταση, πρακτικά είναι αναστρέψιμη και πλήρως ιάσιμη εάν αναγνωρισθεί και αντιμετωπιστεί εγκαίρως2.
Η παθοφυσιολογία του πνευμοθώρακα υπό τάση είναι διαφορετική στους ασθενείς που έχουν αυτόματη αναπνοή με τους ασθενείς υπό μηχανικό αερισμό. Οι ασθενείς με αυτόματη αναπνοή έχουν τη δυνατότητα να αναπτύξουν αρκετούς αντιρροπιστικούς μηχανισμούς έτσι που να προλάβουν ή να καθυστερήσουν την αιμοδυναμική κατάρρευση. Αυτοί οι μηχανισμοί περιλαμβάνουν την αύξηση της αναπνευστικής συχνότητας, την μεταβολή του αναπνεόμενου όγκου και τη διατήρηση της αρνητικής πίεσης στην υπεζωκοτική κοιλότητα. Οι μηχανισμοί αυτοί μπορεί να διατηρήσουν την αρτηριακή πίεση, περιορίζοντας την μετάδοση της υπεζωκοτικής πίεσης στο μεσοθωράκιο και το αντίθετο ημιθωράκιο26. Σταδιακά ωστόσο, καθώς οι αντιρροπιστικοί μηχανισμοί δεν είναι ανεξάντλητοι, ο σύστοιχος πνεύμονας συμπιέζεται και ο αναπνεόμενος όγκος μειώνεται με αποτέλεσμα εκτεταμένη διαταραχή των σχέσεων αερισμού-αιμάτωσης, σημαντική υποξαιμία και τελικά καρδιακή ανακοπή υποξικής αιτιολογίας, η οποία συμβαίνει, στις περισσότερες των περιπτώσεων, πριν την επέλευση σημαντικής μη αντιρροπούμενης αιμοδυναμικής κατάρρευσης31.
Στους ασθενείς υπό μηχανικό αερισμό με θετικές πιέσεις, η συνεχώς αυξανόμενη υπεζωκοτική πίεση, η οποία παραμένει θετική σε όλη τη διάρκεια του αναπνευστικού κύκλου, προκαλεί μείωση της φλεβικής επιστροφής η οποία οδηγεί σε υπόταση και εάν δεν αντιμετωπισθεί σε καρδιακή ανακοπή1,27. Ταυτόχρονα, οι θετικές πιέσεις αερισμού αυξάνουν τη ροή αέρα προς την υπεζωκοτική κοιλότητα, με αποτέλεσμα την ταχύτερη αύξηση της ενδοϋπεζωκοτικής πίεσης26, ενώ η μετατόπιση του μεσοθωρακίου οδηγεί σε συμπίεση της άνω κοίλης φλέβας και περαιτέρω παρακώλυση της φλεβικής ροής25 με τελική κατάληξη την καρδιακή ανεπάρκεια, λόγω θωρακικού εξωκαρδιακού επιπωματισμού και την επέλευση καρδιακής ανακοπής, με συνηθέστερο αρχικό ρυθμό άσφυγμη ηλεκτρική δραστηριότητα (ΑΗΔ)31. Σε μια συστηματική ανασκόπηση η αναφερόμενη συχνότητα της υπότασης (16%) και της καρδιακής ανακοπής (2%) ήταν πολύ μικρότερη. σε ασθενείς με αυτόματη αναπνοή σε σύγκριση με αυτούς υπό μηχανικό αερισμό26.
Στην παρούσα περίπτωση ωστόσο, σε αντίθεση με την πλειονότητα των δημιοσιευμένων περιστατικών27, η κλινική εικόνα του ασθενούς εμφάνισε ταχεία επιδείνωση και τελικά επήλθε γρήγορα ανακοπή, παρά την απουσία υποστήριξης της αναπνοής με θετικές πιέσεις. Τα επεισόδια έντονου βήχα που προηγήθηκαν, πιθανά επιτάχυναν τη διαδικασία επιδείνωσης καθώς οδήγησαν σε σημαντικά υψηλή αύξηση των ενδοθωρακικών πιέσεων, η οποία συνέβαλε στην ταχεία επέκταση του πνευμοθώρακα, παρά την αυτόματη αναπνοή.
Ο έντονος βήχας προκαλεί τεράστια αύξηση των πιέσεων στους αεραγωγούς και έχει ενοχοποιηθεί για την πρόκληση αυτόματου πνευμοθώρακα σε ασθενείς με προϋπάρχουσα παθολογία των πνευμόνων32-34.
Η κλινική εικόνα του πνευμοθώρακα διαφέρει ανάλογα με την αναπνοή (αυτόματη, μηχανική υποστήριξη της αναπνοής)1,26.
Η κλινική εικόνα του πνευμοθώραρα σε ασθενείς που είναι σε εγρήγορση περιλαμβάνει αιφνίδια έναρξη δύσπνοιας, ετερόπλευρο θωρακικό άλγος, μείωση του αναπνευστικού ψιθυρίσματος και τυμπανικότητα κατά την επίκρουση27. Επιπρόσθετα ο πνευμοθώρακας υπό τάση μπορεί να έχει αιμοδυναμική επιβάρυνση, διάταση των φλεβών του τραχήλου, μετατόπιση της τραχείας.
Στους ασθενείς υπό μηχανικό αερισμό υποψία για πνευμοθώρακα υπό τάση θα πρέπει να μπαίνει όταν υπάρχει υποξυγοναιμία, ταχυκαρδία, αιφνίδια έναρξη υπότασης, εμφάνιση υποδόριου εμφυσήματος. Αυτά τα σημεία ακολουθούνται από κυκλοφορική κατάρριψη και μεταγενέστερη καρδιακή ανακοπή με αρχικό ρυθμό ΑΗΔ. Βέβαια μεταξύ των δύο αυτών ακραίων καταστάσεων (ασθενής σε εγρήγορση με αυτόματη αναπνοή και ασθενής κατεσταλμένος υπό μηχανικό αερισμό) υπάρχουν ποικίλες καταστάσεις όσον αφορά το επίπεδο συνείδησης αλλά και τον τρόπο αερισμού.
H διάγνωση του πνευμοθώρακα αν και κλινική δεν είναι πάντα εύκολη και χρειάζεται υψηλού βαθμού υποψία, ειδικά σε αιμοδυναμικά ασταθείς ασθενείς που επείγει η άμεση αποσυμπίεση. Κλασικά κλινικά σημεία όμως μετακίνηση της τραχείας και διάταση των σφαγίτιδων δεν είναι αξιόπιστα και στην πλειονότητα των περιπτώσεων απουσιάζουν27. Σε αιμοδυναμικά σταθερούς ασθενείς, η ακτινογραφία θώρακα μπορεί να επιβεβαιώσει τη διάγνωση. Η χρήση υπερήχου κερδίζει συνεχώς έδαφος έναντι της κλασικής ακτινογραφίας καθώς έχει υψηλού βαθμού ευαισθησία (περίπου 80 – 90%) και μπορεί να πραγματοποιηθεί άμεσα στο κρεβάτι του ασθενούς35-37.
Ο ασθενής μέχρι την έξοδο του από τη χειρουργική αίθουσα είχε ομότιμο αναπνευστικό ψιθύρισμα και στα δύο ημιθωράκια, χωρίς δύσπνοια και χωρίς πόνο. Η μικρή έκταση του πνευμοθώρακα δεν επέτρεψε την εντόπιση μειωμένου αναπνευστικού ψιθυρίσματος, ενώ η χορήγηση οξυγόνου για την πρόληψη της μετεγχειρητικής υποξυγοναιμίας αλλά και των αναλγητικών απέτρεψαν την εμφάνιση πόνου και δύσπνοιας. Ενώ η εξέλιξη του απλού πνευμοθώρακα σε ασθενή που αναπνέει αυτόματα είναι αργή, οι πιέσεις που αναπτύχθηκαν με τον έντονο (κατά πολύ μεγαλύτερες από αυτές του μηχανικού αερισμού), συντέλεσαν στην ταχεία εξέλιξη του απλού πνευμοθώρακα σε πνευμοθώρακα υπό τάση.
Ο πνευμοθώρακας αποτελεί μια από τις επιπλοκές της μεσοθωρακοσκόπησης με συχνότητα περίπου 0,08 – 0,23%21. Εάν αυτό γίνει αντιληπτό σωλήνας θωρακικής παροχέτευσης θα πρέπει να τοποθετείται στο τέλος της επέμβασης. Ασυμπτωματικοί ασθενείς στους οποίους ανιχνεύεται μικρός πνευμοθώρακας στην μετεγχειρητική ακτινογραφία θα πρέπει απλά να παρακολουθούνται.
Ο υπό τάση πνευμοθώρακας ως αιτία πρόκλησης καρδιακής ανακοπής αποτελεί κλασική γνώση προπτυχιακών σπουδών38-40. Είναι επίσης γνωστό ότι σε πρόκληση καρδιακής ανακοπής από πνευμοθώρακα βασική προϋπόθεση για την επίτευξη ROSCμε την εφαρμογή ΚΑΡΠΑ είναι η παροχέτευση του πνευμοθώρακα7. Αναγνωρίζοντας αυτή τη σημαντικότητα το ERC δίνει μεγάλη έμφαση στην αναγνώριση και αντιμετώπιση του πνευμοθώρακα κατά την διάρκεια εφαρμογής ΚΑΡΠΑ2,6. Σύμφωνα με τις κατευθυντήριες οδηγίες για την αναζωογόνηση 2015 του ERC, o πνευμοθώρακας υπό τάση αποτελεί αναστρέψιμο αίτιο καρδιακής ανακοπής, το οποίο θα πρέπει να επιβεβαιώνεται ή να αποκλείεται κατά την διάρκεια ΚΑΡΠΑ3.
Στο συγκεκριμένο ασθενή η διαφορική διάγνωση αρχικά κυμάνθηκε, λόγω του είδους της επέμβασης και της παθολογίας του ασθενούς, μεταξύ πνευμοθώρακα, συνδρόμου άνω κοίλης φλέβας και αιμορραγίας στο μεσοθωράκιο. Η εξέλιξη των γεγονότων δεν άφησε κανένα περιθώριο επιβεβαίωσης ή αποκλεισμού των διαγνωστικών αυτών σκέψεων. Καθοριστικό ρόλο για τη οριστική διάγνωση του πνευμοθώρακα υπό τάση ως αιτία επιδείνωσης της κλινικής εικόνας και διακοπής της καρδιακής λειτουργίας ήταν η αδυναμία αερισμού μετά τη διασωλήνωση στα πλαίσια της ΚΑΡΠΑ41.
Σε ασθενείς με αιμοδυναμική ή αναπνευστική κατάρρευση υπάρχει δυσκολία στη διάγνωση, καθώς τα χρονικά περιθώρια είναι περιορισμένα και η αντιμετώπιση θα πρέπει να είναι άμεση42. Σε αυτούς τους ασθενείς επί υποψίας πνευμοθώρακα θα πρέπει να γίνεται άμεση παροχέτευση του καθώς η αναμονή απεικονιστικών εξετάσεων για επιβεβαίωση του αυξάνει τον κίνδυνο θανάτου του ασθενούς27.
Σε ασθενείς με αιφνίδια επιδείνωση ο πνευμοθώρκακας υπό τάση θα πρέπει να αναγνωρίζεται στα πρώτα πέντε λεπτά κατά την αρχική αξιολόγηση κατά ABCDE3. Επί υψοψίας πνευμοθώρακα υπό τάση θα πρέπει να γίνεται παρακέντηση με βελόνα43, η οποία ακολουθείται με τοποθέτηση σωλήνα θωρακικής παροχέτευσης1,6. Υπάρχουν όμως και αρκετές αναφορές όπου η παρακέντηση με βελόνα δεν ήταν αποτελεσματική στο να διαγνώσει ή να αντιμετωπίσει τον υπό τάση πνευμοθώρακα44-46.
Η παρουσία θωρακοχειρουργών στον χώρο της ανακοπής επέτρεψε την απευθείας τοποθέτηση σωλήνων θωρακικής παροχέτευσης, προσφέροντας, σε συγκρίσιμο χρόνο με τη θωρακοκέντηση, περισσότερο αποτελεσματική αντιμετώπιση.
Ο αρχικός ρυθμός της καρδιακής ανακοπής ήταν ΑΗΔ (μη απινιδώσιμος ρυθμός). Καρδιακή ανακοπή παρουσία μαρτύρων με αρχικό ρυθμό ΑΗΔ συνήθως δεν είναι ισχαιμικής αιτιολογίας, ενώ υπάρχει μεγάλη πιθανότητα ύπαρξης αναστρέψιμης αιτίας, η οποία θα πρέπει να αναγνωρισθεί και να αντιμετωπισθεί για να υπάρξει ROSC47-49. Αν και από τις επιστημονικές εταιρείες έχει δοθεί μεγαλύτερη βαρύτητα στους απινιδώσιμους ρυθμούς, καθώς έχουν και μεγαλύτερη επιβίωση, η ΑΗΔ είναι περισσότερο συχνός αρχικός ρυθμός ενδονοσοκομειακής καρδιακής ανακοπής50,51.
Η αναγνώριση της επιδείνωσης του ασθενούς και η κλήση βοήθειας52, η άμεση έναρξη ΚΑΡΠΑ μετά την επέλευση της καρδιακής ανακοπής και η αναγνώριση και αντιμετώπιση της αναστρέψιμης αιτίας πρόκλησης της2,6 έπαιξε καθοριστικό ρόλο στην επίτευξη ROSC αλλά και στην διατήρηση άθικτης της εγκεφαλικής του λειτουργίας.
ΣΥΜΠΕΡΑΣΜΑΤΑ
Ο πνευμοθώρακας υπό τάση αποτελεί μια σπάνια αλλά δυνητικά θανατηφόρο κατάσταση εάν δεν αναγνωρισθεί και αντιμετωπισθεί γρήγορα. Στα σεμινάρια αναζωογόνησης και τραύματος παρουσιάζονται ακραίες καταστάσεις, όπου η διάγνωση είναι εμφανής και η παρακέντηση με βελόνη εύκολη και αποτελεσματική. Στην καθημερινή κλινική πραγματικότητα όμως, τα πράγματα δεν είναι ιδανικά και μπορεί να υπάρχουν αποκλίνουσες κλινικές εκδηλώσεις, που σχετίζονται με τον ασθενή και τις εκάστοτε καταστάσεις. Η καθυστερημένη διάγνωση και η λανθασμένη θεραπεία μπορεί να έχει καταστροφικές συνέπειες για τον ασθενή. Όταν η καρδιακή ανακοπή συμβεί όποια και να είναι η αιτία της, η αναγνώριση της και η άμεση έναρξη ΚΑΡΠΑ, αποτελούν τη μόνη ελπίδα για την επιβίωση του ασθενούς.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Barton E. Tension pneumothorax. Curr Opin Pulm Med 1999 ; 5:269–74.
- Truhlar A, Deakin CD, Soar J, et al. European Resuscitation Council Guidelines for Resuscitation 2015 Section 4. Cardiac arrest in special circumstances Resuscitation. 2015;95:148-201.
- American College of Surgeons Committee on Trauma: Advanced Trauma Life Support Student Course Manual: Ninth Edition. Chicago, U.S.A: American College of Surgeons; 2012.
- Dooley S, Mansour M. Pneumothoraces post mechanical cardiopulmonary resuscitation:A case series. Respir Care 2015;60:118 –21.
- Sharayah A, Unnikrishnan D, Shukla Tension pneumothorax and diffuse subcutaneous emphysema as a complication of cardiopulmonary resuscitation. BMJ Case Rep. 2017: 1-2.
- Soar j, Nolan j, Böttiger B. European Resuscitation Council Guidelines for Resuscitation 2015 Section 3. Adult advanced life support. Resuscitation 2015;95:100–47.
- Buschmann C, Tsokos M, Kleber C. Tension pneumothorax in unsuccessful cardiopulmonary resuscitation. Rom J Leg Med 2014;22 : 221-3.
- Carlens E. Mediastinoscopy: a method for inspection and tissue biopsy in the superior mediastinum. Dis 1959;36: 343 – 52.
- Cho L. Anesthesia for patients with mediastinal masses in Slinger P Principles and practice of anesthesia for thoracic surgery. Springer Switzerland 2019 pp 251-65.
- Vyas K, Davenport D, Ferraris V, Saha S. Mediastinoscopy: Trends and Practice Patterns in the United States. South Med J. 2013 106: 539–44.
- Paleru C, Danaila O, Bolca C, et al. Complications of mediastinoscopy. Pneumologia. 2009;58:39-40.
- Cata J, Lasala J, Mena G, et al. Anesthetic Considerations for Mediastinal Staging Procedures for Lung Cancer. Journal of Cardiothoracic and Vascular Anesthesia 2018; 32: 893–900.
- Thomsen R. Mediastinoscopy and video-assisted thoracoscopic surgery: Anesthetic pitfalls and complications. Semin Cardiothorac Vasc Anesth 2008;12:128–32.
- Ahmed – Nusrath A, Swanevelder J. Anaesthesia for mediastinoscopy. Continuing Educ Anaesth Crit Care. Pain2007;7:6–9.
- Lohser J, Donington JS, Mitchell JD, et al. Anaesthetic management of major haemorrhage during mediastinoscopy. J Cardiothorac Vasc Anesth 2005; 19: 678–83.
- Royse C, Newman S, Chung F, et al. Development and feasibility of a scale to assess postoperative recovery : The Post-operative Quality Recovery Scale. Anesthesiology 2010; 113:892–905.
- Aldrete J, Kroulik D. A postanesthetic recovery score. Anesth Analg 1970; 49:924 –34.
- Wei B, Bryant A, Minnich D, et al. The safety and efficacy of mediastinoscopy when performed by general thoracic surgeons. Ann Thorac Surg. 2014; 97:1878 -83.
- Furgang F, Saidman L. Bilateral tension pneumothorax associated with mediastinoscopy. J Thorac Cardiovasc Surg 1972 ; 63:329-33
- Weiss A, Salter B, Evans A, et al. Esophageal perforation following cervical mediastinoscopy: a rare serious complication. J Thorac Dis 2015; 7:678-81.
- Park B, Flores R, Downey R, et al. Management of major hemorrhage during mediastinoscopy. J Thorac Cardiovasc Surg 2003; 126:726-31.
- Puhakka Η. Complications of mediastinoscopy. The Journal of Laryngology and Otology 1989; 103 :312-5.
- Hammoud Z, Anderson R, Meyers B, et al. The current role of mediastinoscopy in the evaluation of thoracic disease. Thorac Cardiovasc Surg 1999;118:894-9.
- Lemaire A, Nikolic I, PetersenT, et al. Nine year single center experience with cervical mediastinoscopy: Complications and false negative rate. Ann Thorac Surg 2006; 82:1185–9.
- Yoon J, Choi S, Suh J, et al. Tension pneumothorax, is it a really life threatening condition? J Cardiothorac Surg. 2013; 8:197.
- Leigh-Smith S, Harris T. Tension pneumothorax–time for a re-think? Emerg Med J. 2005 22:8-16.
- Roberts D, Leigh-Smith S, Faris P, et al. Clinical Presentation of Patients With Tension Pneumothorax: A Systematic Review. Ann Surg. 2015; 261:1068-78.
- Phillips S, Falk G. Surgical tension pneumothorax during laparoscopic repair of massive hiatus hernia: a different situation requiring different management. Anaesth Intensive Care 2011; 39: 1120-23.
- Hsu C, Sun S. Iatrogenic pneumothorax related to mechanical ventilation. World J Crit Care Med. 2014; 3:8-14.
- Esteban A, Anzueto A, Frutos F, et al. Characteristics and outcomes in adult patients receiving mechanical ventilation: a 28-day international study. JAMA2002; 287: 345-55.
- Nelson D, Porta C, Satterly S, et al. Physiology and cardiovascular effect of severe tension pneumothorax in a porcine model. J Surg Res. 2013; 184:450-7.
- Dennis Mc Cool D. Global Physiology and Pathophysiology of Cough ACCP Evidence-Based Clinical Practice Guidelines. CHEST 2006; 129:48–53.
- Wang H, Nugent W. Cough-induced bilateral spontaneous pneumothorax. Ann Thorac Surg 2010; 90:1363–5.
- Smith J, Aliverti A, Quaranta M, et al.Chest wall dynamics during voluntary and induced cough in healthy volunteers. J Physiol 2012; 590: 563–74.
- Leigh-Smith S, Davies G. Tension pneumothorax: eyes may be more diagnostic than ears. Emerg Med J.2003; 20:495–496.
- Roberts D, Niven D, James M, et al. Thoracic ultrasonography versus chest radiography for detection of pneumothoraces: challenges in deriving and interpreting summary diagnostic accuracy estimates. Crit Care. 2014; 18:416.
- Ueda Κ, Ahmed W, Ross Α. Intraoperative pneumothorax identified withtransthoracic ultrasound. Anesthesiology 2011; 115:653–5
- Lee S, Se K, Kim Y, et al. Cardiac arrest caused by contralateral tensionpneumothorax during one-lung ventilation. Anesth Pain Med 2020; 15:78-82.
- Ryu S, Na H, Bae J, et al. Cardiac arrest occurred by tension pneumothorax during right thoracotomy. Korean J Anesthesiol 2006; 51: 756-9.
- Han K, Kim H, Byon H, et al. Cardiac arrest induced by tension pneumothorax during ventilating bronchoscopy. Korean J Anesthesiol 2010; 59:123-126.
- Bacon Α, Paix Α, Williamso J, et al. Crisis management during anaesthesia: pneumothorax. Qual Saf Health Care 2005;14:1 – 6.
- McEvoy Μ, Thies Κ, Einav S, et al.Cardiac arrest in the operating room: part 2—special situations in the perioperative period. Anesth Analg 2018; 126:889–903.
- Beaven A, Harrison J, Porter K, et al. Clinical suspicion regarding needle decompression for patients with chest trauma. J par; 2019 :1-6.
- Britten S, Palmer S. Chest wall thickness may limit adequate drainage of tension pneumothorax by needle thoracocentesis. J Accid Emerg Med. 1996; 13: 426–427.
- Cullinane D, Morris J, Bass J, et al. Needle thoracostomy may not be indicated in the trauma patient. Injury 2001; 32:749–52.
- Jones R, Hollingsworth J. Tension pneumothoraces not responding to needle thoracocentesis. Emerg Med J 2002; 19:176–7.
- Myerburg R, Halperi H, Egan D, et al. Pulseless Electric Activity Definition, Causes, Mechanisms, Management, and Research Prioritiesfor the Next Decade: Report From a National Heart, Lung, and Blood Institute Workshop. Circulation 2013;128:2532-41.
- Kauppila J Hantula A, Kortelainen M, et al .Association of initial recorded rhythm and underlying cardiac disease in sudden cardiac arrest. Resuscitation 2018; 122:76–8.
- Bergum D, Haugen B, Nordseth T, et al.Recognizing the causes of in-hospital cardiac arrest. A survival benefit. Resuscitation 2015; 97:91–6.
- Nolan J, Soar J, Smith G. On behalf of the National Cardiac Arrest Audit. Incidence and outcome of in-hospital cardiac arrest in the United Kingdom National Cardiac Arrest Audit. Resuscitation 2014; 85:987–92.
- Bergum D, Nordseth T, Mjolstad O, et al.Causes of in-hospital cardiac arrest – Incidences and rate of recognition . Resuscitation 2015; 87:63–8.
- Barwise Α, Thongprayoon Ch, Gajic O, et al. Delayed rapid response team activation is associated with increased hospital mortality, morbidity, and length of stay in a tertiary care institution. Crit Care Med 2016; 44:54–63.
Author Disclosures:
Authors Pezikoglou I., Fyntanidou B., Foroulis Ch., Amaniti A., Alexiou Ι., Kyparissa M., Palaska E. and Grosomanidis V. have no conflicts of interest or financial ties to disclose.
Corresponding author:
Dr Ioakeim Pezikoglou
Anesthesia and ICU Clinic, AHEPA University Hospital, Thessaloniki, Greece
G Parali 19, 54249, Thessaloniki, Greece
T: 00306946736090
email:









